|
||||
|
|
звонок бесплатный
Наши сотрудники:
[email protected]
Екатерина - специалист по продаже а/м КАМАЗ
 [email protected]
[email protected]






Техника в наличии

Тягач КАМАЗ 44108-6030-24
2014г, 6х6, Евро3, дв.КАМАЗ 300 л.с., КПП ZF9, бак 210л+350л, МКБ,МОБ,рестайлинг.
цена 2 220 000 руб.,

КАМАЗ 4308-6063-28(R4)
4х2,дв. Cummins ISB6.7e4 245л.с. (Е-4),КПП ZF6S1000, V кузова=39,7куб.м., спальное место, бак 210л, шк-пет,МКБ, ТНВД BOSCH, система нейтрализ. ОГ(AdBlue), тент, каркас, рестайлинг, внутр. размеры платформы 6112х2470х730 мм
цена 1 950 000 руб.,

Самосвал КАМАЗ 6520-057
2014г, 6х4,Евро3, дв.КАМАЗ 320 л.с., КПП ZF16, ТНВД ЯЗДА, бак 350л, г/п 20 тонн, V кузова =20 куб.м.,МКБ,МОБ, со спальным местом.
цена 2 700 000 руб.,

Самосвал 6522-027
2014, 6х6, дв.КАМАЗ 740.51,320 л.с., КПП ZF16,бак 350л, г/п 19 тонн,V кузова 12куб.м.,МКБ,МОБ,задняя разгрузка,обогрев платформы.
цена 3 190 000 руб.,
СУПЕР ЦЕНА
на АВТОМОБИЛИ КАМАЗ
| 43118-010-10 (дв.740.30-260 л.с.) | 2 220 000 |
| 43118-6033-24 (дв.740.55-300 л.с.) | 2 300 000 |
| 65117-029 (дв.740.30-260 л.с.) | 2 200 000 |
| 65117-6010-62 (дв.740.62-280 л.с.) | 2 350 000 |
| 44108 (дв.740.30-260 л.с.) | 2 160 000 |
| 44108-6030-24 (дв.740.55,рест.) | 2 200 000 |
| 65116-010-62 (дв.740.62-280 л.с.) | 1 880 000 |
| 6460 (дв.740.50-360 л.с.) | 2 180 000 |
| 45143-011-15 (дв.740.13-260л.с) | 2 180 000 |
| 65115 (дв.740.62-280 л.с.,рест.) | 2 190 000 |
| 65115 (дв.740.62-280 л.с.,3-х стор) | 2 295 000 |
| 6520 (дв.740.51-320 л.с.) | 2 610 000 |
| 6520 (дв.740.51-320 л.с.,сп.место) | 2 700 000 |
| 6522-027 (дв.740.51-320 л.с.,6х6) | 3 190 000 |

подробнее про услугу перегона можно прочесть здесь.

|
Нужны самосвалы? Обратите внимание на Ford-65513-02. |
КАМАЗы в лизинг
ООО «Старт Импэкс» имеет возможность поставки грузовой автотехники КАМАЗ, а так же спецтехники на шасси КАМАЗ в лизинг. Продажа грузовой техники по лизинговым схемам имеет определенные выгоды для покупателя грузовика. Рассрочка платежа, а так же то обстоятельство, что грузовики до полной выплаты лизинговых платежей находятся на балансе лизингодателя, и соответственно покупатель автомобиля не платит налогов на имущество. Мы готовы предложить любые модели бортовых автомобилей, тягачей и самосвалов по самым выгодным лизинговым схемам.Контактная информация.
г. Набережные Челны, Промкомзона-2, Автодорога №3, база «Партнер плюс».
тел/факс (8552) 388373.
Схема проезда
Строение и кристаллизация металлов и сплавов лекция 3 Строение металлов и сплавов. Кристаллизация металлов и сплавов
Кристаллизация металлов и сплавов
Процесс перехода из жидкого или газообразного состояния в твердое, в результате чего образуется кристаллическая решетка и возникают кристаллы, называется кристаллизацией.
Чем объясняется существование при одних температурах жидкого, а при других температурах твердого состояния и почему превращение происходит при строго определенных температурах?
В природе все самопроизвольно протекающие превращения, а следовательно, кристаллизация и плавление обусловлены тем, что новое состояние в новых условиях является энергетически более устойчивым, обладает меньшим запасом энергии.
Энергетическое состояние системы, имеющей огромное число охваченных тепловым движением частиц (атомов, молекул), характеризуется особой термодинамической функцией (F ), называемой свободной энергией, которая определяется:
F= U – TS,
где U – внутренняя энергия системы;
Т - абсолютная температура;
S - энтропия
Можно сказать, что чем больше свободная энергия системы, тем система менее устойчива, и если имеется возможность, то система переходит в состояние, где свободная энергия меньше.
С изменением внешних условий, например температуры, свободная энергия системы изменяется по сложному закону, но различно для жидкого и твердого состояний (рис. 3.1).
Рис. 3.1. Изменение свободной энергии жидкого и кристаллического состояний в зависимости от температуры
Выше температуры Тs меньшей свободной энергией обладает вещество в жидком состоянии, нижеTs– вещество в твердом состоянии. Следовательно, выше Ts вещество должно находиться в жидком состоянии, а ниже Ts – в твердом, кристаллическом.
Очевидно, что при температуре, равной Ts свободные энергии жидкого и твердого состояний равны, металл в обоих состояниях находится в равновесии. Эта температура Ts и есть равновесная или теоретическая температура кристаллизации. Однако, при Ts Fж = Fкр, и процесс кристаллизации (плавления) не может идти, так как при равенстве свободных энергий обеих фаз плавление (кристаллизация) не будут сопровождаться уменьшением свободной энергии.
Для начала кристаллизации необходимо, чтобы процесс был термодинамически выгоден системе и сопровождался уменьшением свободной энергии системы. Их кривых (рис. 3.1) видно, что это возможно только тогда, когда жидкость будет охлаждена ниже точки Ts.
Температура, при которой практически начинается кристаллизация, может быть названа фактической температурой кристаллизации.
Охлаждение жидкости ниже температуры кристаллизации называется переохлаждением.
Обратное превращение из кристаллического состояния в жидкое может произойти только выше температуры Ts, это явление называется перенагреванием.
Величиной или степенью переохлаждения называют разность между теоретической и фактической температурами кристаллизации T = Ts - Tф.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах время – температура (рис. 3.2).
Рис. 3.2. Кривые охлаждения, полученные при кристаллизации металла
Охлаждение металла в жидком состоянии сопровождается плавным понижением температуры и может быть названо простым охлаждением, так как при этом нет качественного изменения состояния. При достижении температур кристаллизации на кривой температура – время появляются горизонтальные площадки (рис.3.2), так как отвод тепла компенсируется выделяющейся при кристаллизации скрытой теплотой кристаллизации.
3.2. Механизм процесса кристаллизации
Процесс кристаллизации состоит из двух элементарных процессов. Первый процесс заключается в зарождении мельчайших частиц кристаллов, которые называются зародышами или центрами кристаллизации. Второй процесс состоит в росте кристаллов из этих центров.
Модель кристаллизации металла в первые 7 секунд охлаждения представлена схемой процесса кристаллизации (рис.3.3) и кинетической кривой кристаллизации (рис.3.4).
Рис. 3.3. Схема процесса кристаллизации
Рис. 3.4. Кинетическая кривая кристаллизации
По мере развития кристаллизации в нем участвуют все большее и большее число кристаллов. Поэтому процесс вначале ускоряется, пока в какой-то момент взаимное столкновение растущих кристаллов начинает заметно препятствовать их росту. Рост кристаллов замедляется еще и потому, что количество жидкости, в которой образуются новые кристаллы, становится все меньше. В процессе кристаллизации, пока кристалл окружен жидкостью, он часто имеет правильную форму, но при столкновении и срастании кристаллов их правильная форма нарушается. Внешняя форма кристалла оказывается зависимой от условий соприкосновения растущих кристаллов. Вот почему кристаллы металла - зерна (кристаллиты) не имеют правильной формы.
Скорость всего процесса кристаллизации количественно определяется двумя величинами: скоростью зарождения центров кристаллизации и скоростью роста кристаллов (рис.3.5).
Рис. 3.5. Зависимость скорости кристаллизации (СК) и скорости зарождения центров кристаллизации (ЧЦ) от степени переохлаждения
Величины оптимального переохлаждения до достижения максимальной скорости кристаллизации (СК) и до образования максимального числа центров кристаллизации (ЧЦ) не совпадают.
Размер образовавшихся кристаллов зависит от соотношения СК и ЧЦ. При большом значении СК и малом значении ЧЦ образуется мало крупных кристаллов. При малых значениях СК и больших ЧЦ образуется большое число мелких кристаллов.
Минимальный размер способного к росту зародыша называется критическим размером зародыша.
studfiles.net
2. Кристаллизация и структура металлов и сплавов. Материаловедение: конспект лекций [litres]
2. Кристаллизация и структура металлов и сплавов
Порядок расположения атомов – тип кристаллической решетки – природное свойство металла, форма кристаллов и их размеры зависят от процесса перехода металла из жидкого состояния в твердое. Процесс образования кристаллов при затвердевании металлов называется кристаллизацией. При кристаллизации металлов выделяется тепло, а при переходе металлов из твердого состояния в жидкое происходит поглощение тепла. Наблюдения с помощью измеряющих температуру проборов за процессом понижения температуры
при переходе металла из жидкого состояния в твердое позволили установить определенную закономерность. Сначала температура понижается равномерно. В начальный период образования кристаллов вследствие выделения скрытой теплоты при формировании кристаллической решетки падение температуры прекращается, и она остается неизменной до полного затвердения металла. После того как весь металл затвердеет, температура снова начинает понижаться. Температура, соответствующая горизонтальной площадке, называется критической. Кристаллизация металлов подобна кристаллизации солей, и этот процесс состоит из двух элементарных процессов, протекающих одновременно. Первый заключается в образовании центров кристаллизации, или зародышей кристаллов, второй – в росте кристаллов из этих центров.
Первый этап – появление зародышей кристаллов металла. Второй этап – по мере остывания металла к зародышам присоединяются все новые и новые атомы жидкого металла, которые группируются в определенном порядке один возле другого, образуя элементарные ячейки кристаллической решетки. Этот процесс продолжается до тех пор, пока не закончится кристаллизация. Причем кристаллы затвердевшего металла имеют неправильную и весьма разнообразную форму, что объясняется условиями кристаллизации.
В процессе кристаллизации увеличивается количество кристаллов – в 1 мм 3 может образоваться свыше 1000 кристаллов. Кристаллы, имеющие неправильную внешнюю форму, называются кристаллитами, или зернами. Чистые металлы относительно редко применяются в машиностроении и других отраслях хозяйственного комплекса. Более широко используются сплавы, состоящие из двух и более элементов (из двух металлов, например меди и цинка, или из металла и неметалла, например железа и углерода). Элементы, входящие в сплав, называются компонентами. В зависимости от расположения атомов в кристаллической решетке различают твердые растворы замещения и твердые растворы внедрения. В твердом растворе замещения атомы растворимого компонента замещаются атомами растворителя, а в твердом растворе внедрения атомы растворителя размещаются между атомами растворимого компонента в наиболее слабых местах элементов кристаллической решетки.
Сплавы, представляющие собой твердые растворы, отличаются ценными свойствами. Они тверже и прочнее, чем входящие в него компоненты.
Компоненты некоторых сплавов при кристаллизации могут входить в химическую связь, образуя химическое соединение. Химические соединения обладают очень высокой твердостью и хорошим электросопротивлением.
Поделитесь на страничкеСледующая глава >
tech.wikireading.ru
2. Процесс кристаллизации расплавов металлов
2.1 Кристаллизация металлов и сплавов
Кристаллизация — переход металла (сплава) из жидкого состояния в твердое — происходит в условиях, когда расплав переходит к термодинамически более устойчивому состоянию с меньшей свободной энергией (свободная энергия кристалла меньше свободной энергии жидкой фазы).
Влияние температуры на свободную энергию жидкой (Gж) и твердой фазы (Gт) показано на рис. 1а.
При температуре плавления Тпл жидкая и твердая фазы существуют одновременно. Реальный процесс кристаллизации протекает при переохлаждении металла ниже теоретической температуры кристаллизации Тпл. Величина ∆Т= Тпл - Ткр называется степенью переохлаждения.
Термические кривые, характеризующие процесс кристаллизации чистых металлов при охлаждении с разной скоростью, приведены на рис. 1 б (v— скорость охлаждения, v1 < v2 < v3).
Вначале, когда металл находится в жидком состоянии, температура системы уменьшается плавно. При достижении температуры Тпл на кривой охлаждения появляется горизонтальная площадка, так как отвод теплоты в окружающую среду компенсируется выделяющейся при кристаллизации скрытой теплотой кристаллизации.
По окончании кристаллизации температура вновь уменьшается плавно. При медленном охлаждении (v1) степень переохлаждения мала, и кристаллизация протекает при температуре, близкой к теоретической температуре кристаллизации Тпл. С увеличением скорости охлаждения степень переохлаждения возрастает, и кристаллизация происходит при более низких температурах.
Рисунок 1. Охлаждение расплава и начало кристаллизации
а — изменение свободной энергии (G) в жидком (G Ж) и твердом (G т) состоянии в зависимости от температуры: Ткр — температура начала кристаллизации; Тпл — температура, при которой жидкая и твердая фазы существуют одновременно; ∆T — степень переохлаждения; б — кривые охлаждения металлов при кристаллизации: ∆T1, ∆T2, ∆T3 — степень переохлаждения при скорости охлаждения v1, v2, v3 соответственно.
Чем «чище» жидкий металл, тем выше температура переохлаждения. Процесс кристаллизации начинается с образования кристаллических зародышей (центров кристаллизации) и продолжается в процессе роста их числа и размеров. С повышением степени переохлаждения увеличиваются число зародышей и скорость кристаллизации. Но при дальнейшем повышении степени переохлаждения скорость роста зародышей и скорость кристаллизации уменьшаются.
Рост кристаллов заключается в присоединении к зародышам все новых атомов из жидкой фазы (рис. 2 а). Центры кристаллизации — зародыши (черные квадраты) — самопроизвольно возникают при переохлаждении металла. Очень маленькие зародыши неустойчивы, возникнув, они растворяются. Чем больше степень переохлаждения, тем устойчивее зародыши, тем меньше их критический размер. Далее зародыши увеличиваются в размере, одновременно появляются новые зародыши.
Пока число зародышей невелико, кристаллы растут свободно и сохраняют правильную геометрическую форму. В местах соприкосновения отдельных кристаллов рост их отдельных граней прекращается, развиваются грани в тех местах, где есть свободная жидкость. В результате кристаллы не имеют правильной геометрической формы. Такие кристаллы называются кристаллитами. Чем больше центров кристаллизации, тем больше образуется кристаллов в данном объеме, тем мельче окончательный размер кристаллов. Однако уменьшение скорости зарождения числа зародышей при критических температурах ограничивает возможность регулирования их размера повышением скорости охлаждения. Рис. 2. Схема кристаллизации металла
С целью регулирования размеров зерен часто применяют искусственное введение в расплав веществ, создающих центры кристаллизации (модифицирование). В технических металлах в качестве центров кристаллизации часто выступают инородные включения (например, шлаковые включения, частички футеровки печи, оксиды металлов).
а — схема роста кристаллов; б — структура дендрита; в — схема образования дендрита; ■ — зародыши; 1, 2, 3 — оси кристаллизации.
В большинстве случаев кристаллизация металлов происходит с большой скоростью (кристаллизация при заливке металла в изложницу, кристаллизация расплава при литье в металлические формы). При ускоренном охлаждении металла кристаллы растут неравномерно. Рост зародышей по одной из осей (в направлении наибольшего градиента температур) значительно опережает рост по другим осям, происходит так называемая дендритная кристаллизация.
Д.К.Чернов, описывая рост дендрита (рис. 2 б), ввел понятие «порядок осей кристаллизации». После образования зародыша его развитие (рис. 2 в) идет в направлении наибольшего градиента температур (ось первого порядка). Увеличение размеров осей первого порядка происходит не только в длину, одновременно увеличивается и ее ширина. В дальнейшем от осей первою порядка под определенными углами начинают расти новые оси, называемые осями второго и третьего порядка.
По мере роста осей более высокого порядка (четвертого, пятого и т.д.) постепенно заполняются все промежутки, ранее занятые жидким металлом, — дендритная кристаллизация замедляется.
Дендритная кристаллизация отчетливо выражена в условиях недостатка жидкого металла для заполнения пространства (поверхностные слои, усадочная раковина) и при наличии примесей и посторонних атомов в расплаве (кристаллизация реальных сплавов).
studfiles.net
Лекция 1 Введение. Кристаллическое строение металлов и сплавов. Кристаллизация сплавов.
КУРС ЛЕКЦИЙ
по дисциплине
«Технология конструкционных материалов»
для студентов специальности
МАШИНЫ И ОБОРУДОВАНИЕ ПРИРОДООБУСТРОЙСТВА
И ЗАЩИТЫ ОКРУЖАЮЩЕЙ СРЕДЫ
ВВЕДЕНИЕ
В современных условиях развития общества одним из самых значимых факторов технического прогресса в машиностроении является совершенствование технологии производства. Коренное преобразование производства возможно в результате создания более совершенных средств труда, разработки принципиально новых технологий.
Развитие и совершенствование любого производства в настоящее время связано с его автоматизацией, созданием робототехнических комплексов, широким использованием вычислительной техники, применением станков с числовым программным управлением. Все это составляет базу, на которой создаются автоматизированные системы управления, становятся возможными оптимизация технологических процессов и режимов обработки, создание гибких автоматизированных комплексов.
Важным направлением научно-технического прогресса является также создание и широкое использование новых конструкционных материалов. В производстве все шире используют сверхчистые, сверхтвердые, жаропрочные, композиционные, порошковые, полимерные и другие материалы, позволяющие резко повысить технический уровень и надежность оборудования. Обработка этих материалов связана с решением серьезных технологических вопросов.
Создавая конструкции машин и приборов, обеспечивая на практике их заданные характеристики и надежность работы с учетом экономических показателей, инженер должен уверенно владеть методами изготовления деталей машин и их сборки. Для этого он должен обладать глубокими технологическими знаниями.
Предметом курса «Технология конструкционных материалов» являются современные рациональные и распространенные в промышленности прогрессивные методы формообразования заготовок и деталей машин. Содержание учебника представлено на принципе единства основных, фундаментальных методов обработки конструкционных материалов: литья, обработки давлением, сварки и обработки резанием. Эти методы в современной технологии конструкционных материалов характеризуются многообразием традиционных и новых технологических процессов, возникающих на их слиянии и взаимопроникновении.
Описание технологических процессов основано на их физической сущности и предваряется сведениями о строении и свойствах конструкционных материалов. Комплекс этих знаний обеспечивает универсальный подход к изучению технологии.
Технически чистые металлы характеризуются низкими прочностными свойствами, поэтому в машиностроении применяют главным образом их сплавы. Сплавы на основе железа называют черными, к ним относят стали и чугуны; на основе алюминия, магния, титана и бериллия, имеющие малую плотность — легкими цветными;
на основе меди, свинца, олова и др.—тяжелыми цветными;
на основе цинка, кадмия, олова, свинца, висмута и других металлов — легкоплавкими цветными; на основе молибдена, ниобия, циркония, вольфрама, ванадия и других металлов — тугоплавкими цветными.
КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
Все металлы в твердом состоянии имеют кристаллическое строение. Атомы в твердом металле расположены упорядоченно и образуют кристаллические решетки. Расстояния между атомами называют параметрами решеток и измеряют в нанометрах. С повышением температуры или давления параметры решеток могут изменяться. Некоторые металлы в твердом состоянии в различных температурных интервалах приобретают различную кристаллическую решетку, что всегда приводит к изменению их физико-химических свойств.
Существование одного и того же металла в нескольких кристаллических формах носит название полиморфизма, или аллотропии. Перестройка кристаллических решеток при критических температурах называется полиморфными превращениями. Полиморфные модификации обозначаются греческими буквами, которые в виде индекса добавляют к символу элемента.
КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ СПЛАВОВ
Под сплавом подразумевается вещество, полученное сплавлением двух элементов или более. Элементами сплава могут быть металлы и неметаллы. Эти элементы называются компонентами сплава. В сплаве кроме основных компонентов могут содержаться и примеси. Примеси бывают полезные, улучшающие свойства сплава, и вредные, ухудшающие его свойства. Примеси бывают случайные, попадающие в сплав при его приготовлении, и специальные, которые вводят для придания ему требуемых свойств.
Кристаллическое строение сплава более сложное, чем чистого металла, и зависит от взаимодействия его компонентов при кристаллизации. Компоненты в твердом сплаве могут образовывать твердый раствор, химическое соединение и механическую смесь.
Твердые растворы — компоненты сплава взаимно растворяются один в другом. В твердом растворе один из входящих в состав сплава компонентов сохраняет присущую ему кристаллическую решетку, а второй компонент в виде отдельных атомов распределяется внутри кристаллической решетки.
Химическое соединение — компоненты сплава вступают в химическое взаимодействие, при этом образуется новая кристаллическа решетка. Компоненты имеют определенное соотношение по массе.
Механическая смесь - компоненты сплава обладают полной взаимной нерастворимостью и имеют различные кристаллические решетки. При этих условиях сплав будет состоять из смеси кристаллов составляющих ее компонентов. Механическая смесь имеет постоянную температуру плавления. Механическая смесь, образовавшаяся одновременной кристаллизацией из расплава, называется эвтектикой; в процессе превращения в твердом состоянии — эвтектоидом.
КРИСТАЛЛИЗАЦИЯ СПЛАВОВ
Процесс перехода сплава из жидкого состояния в твердое с образованием кристаллических решеток (кристаллов) называется первичной кристаллизацией,
Свойства сплавов зависят от образующейся в процессе кристаллизации структуры. Под структурой понимают наблюдаемое кристаллическое строение сплава. Процесс кристаллизации начинается с образования кристаллических зародышей — центров кристаллизации. Скорость кристаллизации зависит от скорости зарождения центров кристаллизации и скорости роста кристаллов: чем больше число образующихся зародышей и скорость их роста, тем быстрее протекает процесс кристаллизации. Структура сплава зависит от формы, ориентировки кристаллических решеток в пространстве и скорости кристаллизации.
Центрами кристаллизации могут быть группы элементарных кристаллических решеток, неметаллические включения и тугоплавкие примеси. Кристаллизация сплава обычно начинается от стенок формы (изложницы). С наибольшей скоростью кристаллы растут в направлении, противоположном отводу теплоты, т. е, перпендикулярно к стенке формы.
Если при кристаллизации рост решеток не ограничивается, то получаются кристаллы неограниченного размера древовидной формы — дендриты. Так как процесс кристаллизации происходит из многих центров кристаллизации, то ветви дендритов при росте могут ограничивать друг друга и искажаться. Кристаллы неправильной формы называются зернами, или кристаллитами. Комплекс зерен — это поликристаллическое тело.
Зерна отличаются различной ориентацией кристаллических решеток; размер зерен составляет 1—104 мкм. Зерна повернуты относительно друг друга на десятки градусов. На границах зерен имеется поврежденный переходный слой толщиной порядка нескольких атомных слоев, свойства и химический состав которого могут отличаться от свойств тела зерна.
Кристаллические решетки зерна могут иметь различные структурные несовершенства: точечные, линейные и поверхностные, которые возникают в результате образования вакансий — мест не занятых атомами; дислоцированных атомов, вышедших из узла решетки; дислокации, возникающих при появлении в кристалле незаконченных атомных плоскостей; примесных атомов, внедренных в кристаллическую решетку.
studfiles.net
Кристаллизация металлов и сплавов Кристаллизация металлов из жидкого состояния
Всякое вещество может находиться в трех агрегатных состояниях: твердом, жидком и газообразном.
Газ Жидкость Твердое тело
В газах отсутствует закономерность в расположении частиц. Твердые кристаллические тела имеют правильное строение, при котором атомы и ионы находятся в узлах кристаллических решеток (ближний порядок), а отдельные ячейки и блоки определенным образом ориентированы по отношению друг к другу (дальний порядок). В жидком металле атомы не расположены хаотично, как в газообразном состоянии, и в то же время в их расположении нет той правильности, которая характерна для твердого кристаллического тела. В жидкостях определенная ориентировка распространяется лишь на небольшое число атомов, образующих так называемые флуктуации. Таким образом, для жидкостей характерен только ближний порядок расположения атомов.
Переход металла из жидкого состояния в твердое при определенной температуре называется кристаллизацией.
Вследствие интенсивного теплового движения атомов ближний порядок динамически неустойчив. При охлаждении жидкости подвижность атомов падает, и вблизи температуры плавления образуются группировки атомов, в которых атомы упакованы, как в кристаллах. Эти группировки являются центрами кристаллизации или зародышами. Такие микрообъемы с правильным расположением атомов, возникнув, могут существовать некоторое время, затем рассасываться и возникать вновь в другом элементарном объеме жидкости. С понижением температуры степень ближнего порядка и размер таких микрообъемов возрастают. Итак, при температурах, близких к температуре плавления, в жидком металле возможно образование небольших группировок (их называют фазовыми флуктуациями), в которых атомы упакованы так же, как и в кристаллах.
Далее происходит рост зародышей в результате перехода атомов из переохлажденной жидкости к кристаллам. Кристалл растет послойно, при этом каждый слой имеет одноатомную толщину.
Механизм кристаллизации
При охлаждении происходит переход стали из жидкого состояния в твердое. Образуется большое число центров кристаллизации, зарождение кристаллов (первая стадия) и дальнейший их рост (вторая стадия).
С увеличением степени переохлаждения возрастает число центров кристаллизации, образующихся в единицу времени. Вокруг образовавшихся центров кристаллизации начинают расти кристаллы. Одновременно в жидкой фазе образуются новые центры кристаллизации.
До тех пор, пока формирующийся вокруг центра кристаллизации кристалл окружен жидким расплавом металла, он имеет правильную геометрическую форму, но при столкновении и срастании кристаллов их правильная форма нарушается, и образуются так называемые кристаллиты – зерна. Рост продолжается только в тех направлениях, где есть свободный доступ «питающей» жидкости. Взаимным ростом кристаллов и объясняется неправильная форма зерен.
Зерно – это кристалл неправильной формы, выросший из одного зародыша. Соседние зерна по своему кристаллическому строению имеют неодинаковую ориентировку решеток. Граница между зернами представляет собой узкую переходную зону шириной 5-10 атомных расстояний с нарушенным порядком расположения атомов. В граничной зоне кристаллическая решетка одного зерна переходит в решетку другого зерна. Неупорядоченное строение переходного слоя усугубляется скоплением в этой зоне дислокаций и повышенной концентрацией примесей.
studfiles.net
Кристаллизация металлов | Материаловедение
Любое вещество может находиться в одном из четырех агрегатных состояний: твердом, жидком, газообразном и плазменном. Агрегатное состояние определяется энергией взаимодействия атомов. Стабильным (равновесным) при определенных внешних условиях является состояние вещества, при котором оно обладает минимумом свободной энергии. Свободная энергия — часть внутренней энергии вещества. Внутренняя энергия вещества — это сумма потенциальной энергии (энергии взаимодействия) и кинетической энергии частиц (тепловые колебания). Часть внутренней энергии, высвобождающаяся при переходе вещества из одного состояния в другое,называется свободной энергией. Чем больше высвободится свободной энергии, тем меньшей энергией будет обладать вещество, тем более стабильно его состояние. Свободную энергию можно представить как аналог потенциальной энергии (рис. 1).
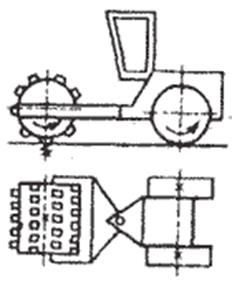
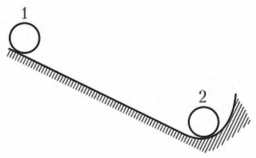 Рисунок 1 - Стремление системы к уменьшению свободной энергии
Рисунок 1 - Стремление системы к уменьшению свободной энергии
В положении 1 шарик имеет максимальную потенциальную энергию. Это положение не является устойчивым, шарик скатывается в положение 2, при котором его потенциальная энергия будет равна 0. Вещество может находиться в метастабильном состоянии (закаленная сталь). Такое состояние не обладает минимумом свободной энергии, но является достаточно устойчивым (стабильным). Вещество в метастабильном состоянии может находиться бесконечно долго при условии постоянства внешних факторов.Первичная кристаллизация металлов и сплавов. Кристаллизация — это переход металла из жидкого состояния в твердое с образованием кристаллического строения. Это первичная кристаллизация (в отличие от вторичной, когда кристаллы металлических фаз выделяются из твердого вещества).Рассмотрение кристаллизации для металлов и сплавов на их основе связано с тем, что эти материалы получают методом литья, тогда как многие неметаллические материалы производят другими способами. Ряд неметаллических материалов существует в природном виде (углерод), многие химические соединения получают путем химических реакций: карбиды — карбидизацией, нитриды — азотированием и т.п. Процесс кристаллизации (затвердевания) обусловлен стремлением системы к переходу в более устойчивое термодинамическое состояние. При изменении внешних условий, например температуры, свободная энергия системы меняется различно для жидкого и твердого (кристаллического) состояния (рис. 2). Выше температуры Ts более стабильнымявляется жидкое состояние, так как металл в этом состоянии имеет меньший запас свободной энергии. Ниже температуры Ts меньшим запасом свободной энергии обладает металл в твердом состоянии. При температуре величины свободных энергий твердого и жидкого состояний равны. Это означает, что металл может находиться в обоих состояниях бесконечно долго, так как переход из одного состояния в другое не будет сопровождаться уменьшением свободной энергии. Температура Ts получила название теоретической температуры кристаллизации.
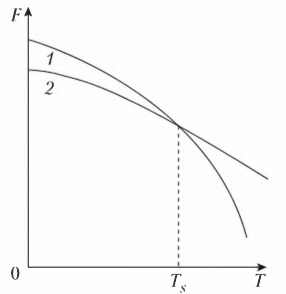 Рисунок 2 - Изменение свободной энергии (Ts) в зависимости от температуры (Т) жидкого (1) и твердого (2) состояния вещества
Рисунок 2 - Изменение свободной энергии (Ts) в зависимости от температуры (Т) жидкого (1) и твердого (2) состояния вещества
Для начала кристаллизации необходимо, чтобы свободная энергия металла в твердом состоянии стала меньше свободной энергии жидкого состояния. Это становится возможным при охлаждении жидкости ниже Ts. Температура, при которой фактически начинается процесс кристаллизации, называется фактической температурой кристаллизации (Тк). Охлаждение жидкого металла ниже теоретической температуры кристаллизации называется переохлаждение, а разность между теоретической и фактической температурой кристаллизации — степенью переохлаждения (ΔТ):
ΔТ=Тs - Тk
Степень переохлаждения зависит от скорости охлаждения жидкого металла. С увеличением скорости охлаждения понижается фактическая температура кристаллизации и, следовательно, возрастает степень переохлаждения. Процесс кристаллизации можно описать с помощью кривых охлаждения, построенных в координатах «температура — время» (рис. 3). Охлаждение в жидком состоянии сопровождается плавным понижением температуры (участок 1 кривой охлаждения), при достижении температуры кристаллизации на кривой охлаждения появляется горизонтальная площадка (участок 2 кривой охлаждения), т.е. охлаждение (понижение температуры) останавливается. Это вызвано тем, что отвод тепла компенсируется выделяющейся в процессе кристаллизации скрытойтеплотой кристаллизации. После полного перехода металла из жидкого состояния в твердое температура вновь начинает плавно снижаться (участок 3 кривой охлаждения). Увеличение скорости охлаждения от V1 до V3 приводит к увеличению степенипереохлаждения (см. рис. 3).
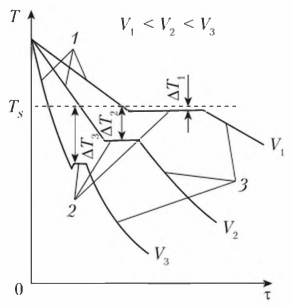 Рисунок 3 - Кривые охлаждения металла
Рисунок 3 - Кривые охлаждения металла
Кристаллизация начинается с образования в жидком металле центров кристаллизации и продолжается за счет роста их числа и размеров (рис. 4). Процесс кристаллизации можно охарактеризовать двумя параметрами: числом центров кристаллизации (ЧЦК),
 Рисунок 4- Схема процесса кристаллизации
Рисунок 4- Схема процесса кристаллизации
образующихся в единицу времени в единице объема (1 см3/с), и скоростью роста кристаллов (СК ) [мм /с]. Эти параметры зависят от степени переохлаждения, а следовательно, от скорости охлаждения при кристаллизации металла. В соответствии с законом Таммана для каждой степени переохлаждения указанные параметры могут иметь только одно значение (рис. 5).При теоретической температуре кристаллизации ( Ts) значения ЧЦК и СК равны 0 и кристаллизация происходить не может. При повышении степени переохлаждения значения ЧЦК и СК возрастают, процесс кристаллизации идет быстро. Это объясняется тем, что при высоких температурах, близких к Тs подвижность атомов велика. При определенных степенях переохлаждения значения ЧЦК и СК достигают максимума, после чего снижаются вследствие уменьшения подвижности атомов при низких температурах.
Размер образовавшихся в процессе кристаллизации зерен зависит от соотношения величин ЧЦК и СК, т.е. определяется степенью переохлаждения (скоростью охлажденияметалла в процессе кристаллизации). При малых степенях переохлаждения (низкой скорости охлаждения металла) образуется малое число центров кристаллизации, которыерастут с большой скоростью,---- АТ' (см. рис. 5). В этом случае структура металла после окончания кристаллизации будет крупнозернистой. При больших степенях переохлаждения, напротив, ЧЦК велико, а СК мала (ДГ" - АТ”'), поэтому структура металла получается мелкозернистой.Если степень переохлаждения настолько велика, что значения ЧЦК и СК близки к пулю, кристаллизации не происходит. При этом образуется твердое тело, имеющее не кристаллическое строение с «правильным» расположением атомов, а аморфное — с хаотическим расположением атомов — «твердая жидкость». Аморфное состояниехарактерно для неметаллических материалов (стекла, полимеры). Для получения аморфного состояния у металлических материалов требуется очень большая скорость охлаждения 106... 107 °С/с.
matved.ru
Строение и кристаллизация металлов и сплавов лекция 3 Строение металлов и сплавов
ТЕМА: СТРОЕНИЕ И КРИСТАЛЛИЗАЦИЯ МЕТАЛЛОВ И СПЛАВОВ
Лекция 3
3.1. Строение металлов и сплавов
Любое вещество может находиться в трех агрегатных состояниях: твердом, жидком, газообразном. Возможен переход из одного состояния в другое, если новое состояние в новых условиях является более устойчивым, обладает меньшим запасом энергии.
С изменением внешних условий свободная энергия изменяется по сложному закону различно для жидкого и кристаллического состояний. Характер изменения свободной энергии жидкого и твердого состояний с изменением температуры показан на рис. 3.1.
Рис. Изменение свободной энергии в зависимости от температуры
В соответствии с этой схемой выше температуры ТS вещество должно находиться в жидком состоянии, а ниже ТS – в твердом.
При температуре равной ТS жидкая и твердая фаза обладают одинаковой энергией, металл в обоих состояниях находится в равновесии, поэтому две фазы могут существовать одновременно бесконечно долго. Температура ТS – равновесная или теоретическая температура кристаллизации.
Рассмотрим переход металла из жидкого состояния в твердое.
При нагреве всех кристаллических тел наблюдается четкая граница перехода из твердого состояния в жидкое. Такая же граница существует при переходе из жидкого состояния в твердое.
Кристаллизация – это процесс образования участков кристаллической решетки в жидкой фазе и рост кристаллов из образовавшихся центров.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах время – температура. Кривая охлаждения чистого металла представлена на рис. 3.2.
Рис. Кривая охлаждения чистого металла
– теоретическая температура кристаллизации;
. – фактическая температура кристаллизации.
3.2. Механизм и закономерности кристаллизации металлов
При соответствующем понижении температуры в жидком металле начинают образовываться кристаллики – центры кристаллизации или зародыши.
Механизм кристаллизации представлен на рис.3.4.
Рис.3.4. Модель процесса кристаллизации
Центры кристаллизации образуются в исходной фазе независимо друг от друга в случайных местах. Сначала кристаллы имеют правильную форму, но по мере столкновения и срастания с другими кристаллами форма нарушается. Рост продолжается в направлениях, где есть свободный доступ питающей среды. После окончания кристаллизации имеем поликристаллическое тело.
3.3. Понятие об изотропии и анизотропии
Свойства тела зависят от природы атомов, из которых оно состоит, и от силы взаимодействия между этими атомами. Силы взаимодействия между атомами в значительной степени определяются расстояниями между ними. В аморфных телах с хаотическим расположением атомов в пространстве расстояния между атомами в различных направлениях равны, следовательно, свойства будут одинаковые, то есть аморфные тела изотропны
В кристаллических телах атомы правильно располагаются в пространстве, причем по разным направлениям расстояния между атомами неодинаковы, что предопределяет существенные различия в силах взаимодействия между ними и, в конечном результате, разные свойства. Зависимость свойств от направления называется анизотропией
3.4. Аллотропия или полиморфные превращения
Способность некоторых металлов существовать в различных кристаллических формах в зависимости от внешних условий (давление, температура) называется аллотропией или полиморфизмом.
Каждый вид решетки представляет собой аллотропическое видоизменение или модификацию.
Примером аллотропического видоизменения в зависимости от температуры является железо (Fe).
Fe: – ОЦК - ;
– ГЦК - ;
– ОЦК - ; (высокотемпературное )
Превращение одной модификации в другую протекает при постоянной температуре и сопровождается тепловым эффектом. Видоизменения элемента обозначается буквами греческого алфавита в виде индекса у основного обозначения металла.
Примером аллотропического видоизменения, обусловленного изменением давления, является углерод: при низких давлениях образуется графит, а при высоких – алмаз.
3.5. Магнитные превращения
Некоторые металлы намагничиваются под действием магнитного поля. После удаления магнитного поля они обладают остаточным магнетизмом. Это явление впервые обнаружено на железе и получило название ферромагнетизма. К ферромагнетикам относятся железо, кобальт, никель и некоторые другие металлы.
При нагреве ферромагнитные свойства металла уменьшаются постепенно: вначале слабо, затем резко, и при определ¨нной температуре (точка Кюри) исчезают (точка Кюри для железа – ). Выше этой температуры металлы становятся парамагнетиками. Магнитные превращения не связаны с изменением кристаллической решетки или микроструктуры, они обусловлены изменениями в характере межэлектронного взаимодействия.
3.6. Понятие о сплавах и методах их получения
Под сплавом понимают вещество, полученное сплавлением двух или более элементов. Возможны другие способы приготовления сплавов: спекания, электролиз, возгонка. В этом случае вещества называются псевдосплавами.
Сплав, приготовленный преимущественно из металлических элементов и обладающий металлическими свойствами, называется металлическим сплавом.
Основные понятия в теории сплавов.
Компоненты – вещества, образующие систему. В качестве компонентов выступают чистые вещества и химические соединения.
Фаза – однородная часть системы, отделенная от других частей системы поверхностного раздела, при переходе через которую структура и свойства резко меняются.
3.7. Особенности строения, кристаллизации и свойств сплавов: механических смесей, твердых растворов, химических соединений
Строение металлического сплава зависит от того, в какие взаимодействия вступают компоненты, составляющие сплав. Почти все металлы в жидком состоянии растворяются друг в друге в любых соотношениях. При образовании сплавов в процессе их затвердевании возможно различное взаимодействие компонентов.
В зависимости от характера взаимодействия компонентов различают сплавы:
механические смеси;
химические соединения;
твердые растворы.
Сплавы механические смеси образуются, когда компоненты не способны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения.
Образуются между элементами значительно различающимися по строению и свойствам, когда сила взаимодействия между однородными атомами больше чем между разнородными. Сплав состоит из кристаллов входящих в него компонентов (рис. 4.1). В сплавах сохраняются кристаллические решетки компонентов.
Рис. Схема микроструктуры механической смеси
Сплавы химические соединения образуются между элементами, значительно различающимися по строению и свойствам, если сила взаимодействия между разнородными атомами больше, чем между однородными.
Особенности этих сплавов:
Постоянство состава, то есть сплав образуется при определенном соотношении компонентов, химическое соединение обозначается Аn Вm/
Образуется специфмческая, отличающаяся от решеток элементов, составляющих химическое соединение, кристаллическая решетка с правильным упорядоченным расположением атомов (рис. 4.2)
Ярко выраженные индивидуальные свойства
Постоянство температуры кристаллизации, как у чистых компонентов
Рис. Кристаллическая решетка химического соединения
Сплавы твердые растворы – это твердые фазы, в которых соотношения между компонентов могут изменяться. Являются кристаллическими веществами.
Характерной особенностью твердых растворов является:наличие в их кристаллической решетке разнородных атомов, при сохранении типа решетки растворителя.
Твердый раствор состоит из однородных зерен (рис. 4.3).
Рис. Схема микроструктуры твердого раствора
3.7. Кристаллизация сплавов
Кристаллизация сплавов подчиняется тем же закономерностям, что и кристаллизация чистых металлов. В сплавах в твердых состояниях, имеют место процессы перекристаллизации, обусловленные аллотропическими превращениями компонентов сплава, распадом твердых растворов, выделением из твердых растворов вторичных фаз, когда растворимость компонентов в твердом состоянии меняется с изменением температуры.
Эти превращения называют фазовыми превращениями в твердом состоянии.
При перекристаллизации в твердом состоянии образуются центры кристаллизации и происходит их рост.
Обычно центры кристаллизации возникают по границам зерен старой фазы, где решетка имеет наиболее дефектное строение, и где имеются примеси, которые могут стать центрами новых кристаллов. У старой и новой фазы, в течение некоторого времени, имеются общие плоскости. Такая связь решеток называется когерентной связью. В случае различия строения старой и новой фаз превращение протекает с образованием промежуточных фаз.
Нарушение когерентности и обособления кристаллов наступает, когда они приобретут определенные размеры.
Процессы кристаллизации сплавов изучаются по диаграммам состояния.
refdb.ru
423800, Набережные Челны , база Партнер Плюс, тел. 8 800 100-58-94 (звонок бесплатный)