Содержание
польза обработки, как происходит процедура
Специальная обработка металла позволяет упрочнить поверхность, а также придать ей нужные эксплуатационные характеристики. Общее название процедуры — операция улучшения поверхностных слоев, что сразу объясняет суть обработки. Цианирование в отдельных случаях является единственным оправданным способом улучшения свойств металла. Среди химико-термических методов обработки именно данный способ самый распространенный благодаря своей простоте и невысокой стоимости. Всего за несколько часов характеристики изделия существенно улучшаются при соблюдении всех требований к выполнению операции.
Содержание
- 1 Что такое цианирование
- 1.1 Польза
- 1.2 Особенности процедуры
- 2 Диффузия веществ в поверхностные слои
- 3 Как происходит цианирование
- 3.1 Эффективность
- 4 Преимущества и недостатки обработки
- 5 Сульфоцианирование
- 6 Какая температура цианирования лучше
- 7 Итог
Что такое цианирование
Процедурой цианирования называют насыщение поверхности разных металлических сплавов одновременно углеродом и азотом. В зависимости от использования основных материалов процессы могут называться совершенно по-разному. Если поверхность обрабатывается под воздействием газов, то такая процедура называется нитроцементацией. Цианирование предполагает обработку металла с использованием расплавленных солей. Чаще всего для этих целей используют цианистый натрий либо кальций. В больших электрованнах смесь расплавляется и ее температура поддерживается на протяжение всей процедуры.
В зависимости от использования основных материалов процессы могут называться совершенно по-разному. Если поверхность обрабатывается под воздействием газов, то такая процедура называется нитроцементацией. Цианирование предполагает обработку металла с использованием расплавленных солей. Чаще всего для этих целей используют цианистый натрий либо кальций. В больших электрованнах смесь расплавляется и ее температура поддерживается на протяжение всей процедуры.
Польза
Цианирование стали достаточно распространенная процедура, которая используется для улучшения свойств изделий, использующихся в различных сферах промышленности. Благодаря обработке можно достигнуть:
- повышения износостойкости поверхности детали;
- увеличения твердости;
- повышения уровня выносливости металла, при возникновении различных повреждений деталь сохранит свой функционал.
На цианированных поверхностях отмечается меньшее налипание материала, из-за чего снижается коэффициент трения при попадании стружки в механизмы. В среднем стойкость цианированных инструментов увеличивается в 1,5-2 раза. Целей проведения цианирования может быть очень много, а благодаря тщательно выверенному технологическому процессу большинство из них можно достаточно легко достигнуть.
В среднем стойкость цианированных инструментов увеличивается в 1,5-2 раза. Целей проведения цианирования может быть очень много, а благодаря тщательно выверенному технологическому процессу большинство из них можно достаточно легко достигнуть.
Особенности процедуры
Цианирование выполняется на сталях различных марок, в том числе и на нержавейке. В зависимости от температурного режима, который соблюдался во время самой процедуры, улучшаются прочностные и эксплуатационные характеристики деталей. В зависимости от целей могут подбираться способы цианирования, а также состав смесей. Неправильный подбор технологии может стать причиной изменений отдельных характеристик в худшую сторону.
Диффузия веществ в поверхностные слои
В процессе цианирования происходит насыщение стали азотом и углеродом, за счет диффузии веществ в структуру металла. Поверхностный диффузионный слой предполагает изменение в своём составе показателей азота и углерода. Если при нагревании показатели азота существенно снижаются, то углерода — повышаются. Количество углерода в слое может повышаться непрерывно либо до нужного момента. Количество углерода также может снижаться на последних этапах обработки металла.
Количество углерода в слое может повышаться непрерывно либо до нужного момента. Количество углерода также может снижаться на последних этапах обработки металла.
Благодаря таким особенностям степень насыщения поверхностного слоя может фиксироваться при различных температурных режимах цианирования. Также на степень насыщения существенное влияние оказывают особенности среды, где происходит обработка металлического сплава.
На особенности обработки сильно влияет азот, который напрямую воздействует на следующие параметры:
- глубину металлического слоя, на которой будут происходить диффузионные процессы;
- степень насыщенности слоя углеродом.
Очень важно подобрать соотношение всех составляющих в смеси для цианирования, так как при повышенном содержании азота диффузия будет происходить малоактивно, что приведет к образованию на поверхности металла различных образований. Правильно смешанный состав позволит достичь нужного результата при минимальных потерях.
Насыщение металлического сплава азотом и углеродом происходит в две стадии, которые сильно отличаются друг от друга. На первой стадии поверхностный слой насыщается одновременно двумя элементами, длительность этапа составляет от 1 до 3 часов. На втором этапе атомы азота могут переходить обратно в форму газа и выходить наружу. В данное время поверхностный слой продолжает насыщаться углеродом.
Особенностью цианирование стали выступает то, что углерод в процессе обработки проникает на меньшую глубину, в отличие от азота. Глубина проникновения веществ зависит только от структуры обрабатываемого материала. Стоит учесть, что изделия с небольшой толщиной могут иметь более высокие показатели хрупкости в отличие от деталей со стандартной толщиной.
Как происходит цианирование
Самый популярный вариант цианирования — низкотемпературная обработка. Метод применим для деталей и инструментов из быстрорежущих сталей. Сама процедура выполняется при температуре всего в 550-570 градусов по Цельсию в соляных ваннах.
Варианты цианистых ванн:
- 50% цианистого калия и 50% цианистого натрия. Средняя температура плавления смеси около 490°С.
- 96—98% цианистого натрия и 4—2% соды. Смесь плавится при температуре 550°С.
- 60% цианистого натрия и 40% соды. Температура плавления состава около 440°С.
Первые две смеси достаточно густые. Последняя смесь, в состав которой входит натрий и сода, отличается более жидкой формой и отсутствием прилипания солей к металлической поверхности. Благодаря этим факторам последняя смесь используется гораздо чаще, чем остальные две.
Цианирование стали может проводиться исключительно после термической обработки металла и конечной его заточки. В процессе обработки стали детали погружаются в ёмкость с солями в жидком состоянии. Для этого чаще всего используются специальные крючки либо проволока, размер которых зависит от объема и веса детали. Время выдержки стальной детали составляет от 5 до 30 минут. После поднятия стальной детали из ёмкости на металле образовывается цианированный слой, толщина которого составляет 0,02-0,07 мм. Верхняя часть слоя имеет достаточно небольшую толщину, поэтому он очень быстро стирается в процессе эксплуатации. Внутренняя часть имеет большие прочностные характеристики, а также повышенную износостойкость.
Верхняя часть слоя имеет достаточно небольшую толщину, поэтому он очень быстро стирается в процессе эксплуатации. Внутренняя часть имеет большие прочностные характеристики, а также повышенную износостойкость.
Эффективность
Эффективность цианирования хоть и подтверждена, но не имеет единого показателя. Всё зависит не только от качества обработки, но и от способа переточки деталей, а также их характера износа. Наибольшая эффективность цианирования отмечается при обработке следующих инструментов:
- резьбовых и червячных фрез;
- фасонных резцов и метчиков;
- долбяков.
В процессе точки выполняется переточка исключительно по передней поверхности. Высокая эффективность обработки поверхности отмечается у сверл и зенкеров благодаря сохранению цианированного слоя на передних поверхностях и дополнительных режущих лезвий. Так как при переточке шлицевых фрез и отрезных резцов полностью удаляется слой, то после точки необходимо подвергать изделия повторной обработке.
Также стоит учесть, что цианирование способно увеличить хрупкость зубчиков детали. Так как материал изнашивается не только по задней стенке, то в будущем слой может выполнять роль абразива, что приведет к преждевременному изменению стойкости детали. Прежде, чем выполнять цианирование необходимо тщательно продумать где будет располагаться деталь.
Преимущества и недостатки обработки
Положительная сторона цианирования — весь процесс происходит при относительно невысоких температурах. Это позволяет не изнашивать используемое оборудование и предотвращать возникновение деформаций в обрабатываемых деталях.
После обработки структура отличается большей устойчивостью к различным повреждениям. Именно обработка при помощи цианирования позволяет в дальнейшем применять способ закаливания низколегированных сталей в масле. Остаточный аустенит, который присутствует в изделиях из стали, подвергшихся цианированию, обеспечивает улучшение параметров по следующим характеристикам:
- пластичность;
- ударная вязкость;
- прочность на изгиб.

Именно благодаря этим характеристикам цианированию могут подвергаться детали, которые в дальнейшем будут эксплуатироваться в условиях повышенных нагрузок.
Один из главных недостатков цианирования — после сложной обработки защитный слой может составлять всего 0,7-0,8 миллиметров. Так как в процессе работы используется азотированная и науглероживанная атмосфера, что очень важно контролировать количество этих материалов в воздухе, а также при необходимости проветривать помещение.
Сульфоцианирование
Данная обработка в большей степени напоминает процесс цианирования. Поверхность насыщается не только углеродом и азотом, но также и серой. Сульфоцианированные детали в большей степени обладают такими же характеристиками как и цианированные. Лучше всего сульфоцианированные детали показали себя в механизмах на средних нагрузках. Благодаря немного другой схеме цианирования предупреждается схватывание и наволакивание металла.
Нормальная температура плавления смеси составляет 560-580 градусов. Обработку стальных сплавов проводят преимущественно в жидких средах, но также возможно и в газовых. Так как сульфоцианированные детали обладают чуть большей прочностью, то их использование оправданно в качестве поршневых колец, чугунных втулок, разнообразных запчастей насоса.
Обработку стальных сплавов проводят преимущественно в жидких средах, но также возможно и в газовых. Так как сульфоцианированные детали обладают чуть большей прочностью, то их использование оправданно в качестве поршневых колец, чугунных втулок, разнообразных запчастей насоса.
Какая температура цианирования лучше
Важно учитывать многие факторы, которые будут влиять на эксплуатацию прибора. При низкотемпературном цианировании металл нагревается на минимальных показателях. Горячее цианирование предлагает использование ванн со средней температурой около 850 градусов.
В среднем цианирование занимает до 6 часов, поэтому первый результат видно достаточно быстро. На низких температурах происходит меньше деформации, поэтому изделия сохраняют свою геометрию и функциональность. В отдельных случаях бывает недостаточно низких температур, поэтому рекомендуется использование цианированных деталей горячим способом.
Итог
Цианирование — важная технологическая операция для улучшения эксплуатационных характеристик изделий из различных марок стали. Цианирование экономически оправданная процедура, которая актуальна для обработки материалов в промышленности.
Цианирование экономически оправданная процедура, которая актуальна для обработки материалов в промышленности.
Используемая литература и источники:
- Физико-химические основы раскисления стали / А.М.Самарин. — М.: Издательство Академии Наук СССР
- Аналитическая химия благородных металлов (комплект из 2 книг) / Ф. Бимиш. — М.: Мир
- Статья на Википедии
Современные технологии: цианирование стали
12
Март
Процесс “Цианирование” — процесс химико-термической обработки, заключающийся в диффузионном насыщении поверхностного слоя стали одновременно углеродом и азотом. Целью цианирования является получение высокой твердости и износостойкости поверхности деталей с сохранением пластичной сердцевины.
Цианирование проводится в жидких и газовых средах.
Жидкостное цианирование заключается в нагреве деталей в расплавленных солях, содержащих цианистый натрий (NaCN). 60.
60.
Для получения слоя глубиной от 0,2 до 1,5лш цианирование ведут при 900—950° С с выдержкой от 30 мин до 5 ч в цианистых ваннах, содержащих 3—8% NaCN, < 30% NaCl, > 30% ВаС12, < 40% ВаС03 (рабочий состав ванны). При нагреве в ванне происходят следующие реакции:
2NaCN + BaCl2 = 2NaCl + Ва (CN)2 Ba(CN)2 = BaCN2 + C BaCN2 + 02 = BaO + CO + 2N
Образующиеся атомарный углерод и азот диффундируют в сталь. Цианированный слой содержит 0,8—1,2% углерода и 0,2—0,3% азота. При высокой температуре цианирования (900—950° С) происходит рост зерна аустенита. Поэтому детали после цианирования непосредственной закалке не подвергаются, а охлаждаются на воздухе, а затем производится закалка и низкий отпуск.
Низкотемпературное цианирование применяют для повышения поверхностной твердости, износостойкости и предела выносливости деталей из конструкционных сталей и для повышения стойкости инструмента из быстрорежущей стали.
Низкотемпературное цианирование деталей из конструкционных сталей, называемое также «мягким азотированием», проводят при 560—580° С в цианистых ваннах, содержащих до 60% NaCN. Время выдержки в ванне 1—3 ч, максимальная рациональная глубина слоя 0,15 мм. Диффундирует в сталь преимущественно азот. Твердость цианированного слоя HV = 300—800 (в зависимости от стали). Перед низкотемпературным цианированием производится полная механическая и термическая обработка деталей.
Время выдержки в ванне 1—3 ч, максимальная рациональная глубина слоя 0,15 мм. Диффундирует в сталь преимущественно азот. Твердость цианированного слоя HV = 300—800 (в зависимости от стали). Перед низкотемпературным цианированием производится полная механическая и термическая обработка деталей.
Недостатком жидкостного цианирования является сильная ядовитость цианистых солей. Поэтому цианистые ванны устанавливают в отдельном помещении, с вентиляцией у каждой ванны. При работе на цианистых ваннах требуется большая осторожность и тщательное соблюдение всех правил техники безопасности. Жидкостное цианирование проводится в цианистых ваннах, которые целесообразно устанавливать в поточную линию.
Влияние цианида на сталь и то, как минералы железа выщелачиваются растворами цианида
Коррозия черного проката мягкой стали в растворе цианида натрия незначительна. Кусок стали, взвешенный в растворе цианида натрия, поддерживаемом при 0,05% NaCN и 0,001% CaO в присутствии воздуха, потерял 0,002% своего веса за две недели, что было эквивалентно проникновению 0,76 микрона в год. Окисленное железо минералы, такие как гематит, магнетит, гетит, сидерит и минералы силиката железа, практически не подвержены влиянию растворов цианидов. Говорят, что сложные минералы карбоната железа, такие как анкерит, в некоторой степени разлагаются в растворах цианидов с низкой щелочностью (ниже pH 10) с образованием ферроцианидов. Сульфидные минералы железа заметно разлагаются в растворах цианидов, однако степень разложения зависит от конкретного сульфидного минерала, размера частиц и условий растворения.
Окисленное железо минералы, такие как гематит, магнетит, гетит, сидерит и минералы силиката железа, практически не подвержены влиянию растворов цианидов. Говорят, что сложные минералы карбоната железа, такие как анкерит, в некоторой степени разлагаются в растворах цианидов с низкой щелочностью (ниже pH 10) с образованием ферроцианидов. Сульфидные минералы железа заметно разлагаются в растворах цианидов, однако степень разложения зависит от конкретного сульфидного минерала, размера частиц и условий растворения.
Тремя наиболее важными минералами железа в цианировании являются пирит, марказит и пирротин. Эти минералы разлагаются в растворах цианидов в указанном порядке, т. е. пирит наиболее устойчив, а пирротин наименее. Пирит, FeS2, нерастворим в соляной кислоте, но легко разлагается в азотной кислоте, при этом большая часть серы переходит в серную кислоту. Марказит имеет ту же химическую формулу, что и пирит, но другую кристаллическую форму. Он тускнеет и разлагается гораздо легче, чем пирит. Соляная кислота на него практически не действует. Азотная кислота легко разлагает марказит, большая часть серы выделяется в свободном состоянии; в этом отношении он отличается от пирита. Пирротин варьирует по химическому составу от Fe5S6 до Fe16S17; говорят, что это сульфид железа, FeS, содержащий различное количество растворенной серы. Пирротин растворяется в разбавленной соляной кислоте, выделяя сероводород и оставляя элементарную серу, например:
Соляная кислота на него практически не действует. Азотная кислота легко разлагает марказит, большая часть серы выделяется в свободном состоянии; в этом отношении он отличается от пирита. Пирротин варьирует по химическому составу от Fe5S6 до Fe16S17; говорят, что это сульфид железа, FeS, содержащий различное количество растворенной серы. Пирротин растворяется в разбавленной соляной кислоте, выделяя сероводород и оставляя элементарную серу, например:
Fe7S8 + 14 HCl = 7 FeCl2 + 7 h3S + S
Иногда минералы сульфида железа тесно связаны с такими минералами, как мелантерит, FeSO4*7h3O. Этот минерал растворим в воде и легко реагирует с цианидом.
Разложение сульфидов железа в воде, щелочах и растворах цианидов было предметом многочисленных исследований и предположений. Было проведено более фундаментальное исследование разложения пирита в различных растворах, чем марказита или пирротина. Последние минералы более изучены в реальных рудах благородных металлов, чем в простых системах, состоящих из чистого минерала и раствора. Поскольку пирротин часто ассоциируется с другими сульфидными минералами в рудах драгоценных металлов, такими как арсенопирит, халькозин и т. д., могут существовать некоторые сомнения относительно того, можно ли приписать определенный эффект при цианировании исключительно пирротину.
Поскольку пирротин часто ассоциируется с другими сульфидными минералами в рудах драгоценных металлов, такими как арсенопирит, халькозин и т. д., могут существовать некоторые сомнения относительно того, можно ли приписать определенный эффект при цианировании исключительно пирротину.
При 100 граммах минус 200 меш пирита высокого качества и 30 мл. дистиллированной воды перемешивали на вальцах в течение 25 минут и фильтровали, в фильтрате оказалось 0,736 г. железного купороса. Вторая обработка того же пирита свежей дистиллированной водой показала, что в фильтрате содержится 0,030 г. железного купороса, а третья обработка дала только 0,009 г. железного купороса. Количество сульфат-иона в растворе было больше эквивалента всего железа в растворе. Это указывает на то, что часть сульфата железа гидролизуется до серной кислоты и гидроксида железа. Считалось, что последний адсорбируется в виде покрытия на поверхности пирита, что замедляет дальнейшее разложение пирита. Подобные эксперименты, проведенные на пирите с различными размерами сит, показали, что количество сульфата железа, обнаруженного в растворе, зависит от открытой поверхности пирита.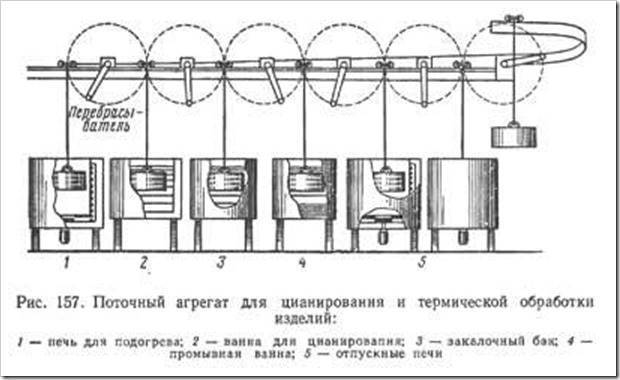
В результате воздействия извести и воздуха на пиритную флотационную пульпу образовались растворимые сульфиды, тиосульфаты и незначительное количество коллоидной серы. Растворенный кислород и растворимые сульфиды вступают в реакцию с образованием тиосульфата и сульфата. В присутствии пирита растворенный кислород и тиосульфат взаимодействовали с образованием сульфата. В отсутствие пирита растворы тиосульфата кальция не изменялись при аэрации. При подщелачивании известью они также оставались неизменными, а при подкислении разлагались. Результаты длительного оксигенирования тонкодисперсного пирита в известковом растворе показали, что едкость вначале быстро падала, а затем медленнее; максимальные количества растворимых восстановителей – сульфида кальция и тиосульфата кальция – образуются при приближении щелочности к нулю (рН 8). По-видимому, присутствие гидроксида кальция было необходимо для образования растворимых сульфидов. Ниже рН 8 восстановители быстро исчезают, и единственным продуктом, образующимся при действии кислорода на пирит, является сульфат, в основном серная кислота.
Для исследования реакций, протекающих в системе пирита, гидроксида натрия и воздуха, была принята следующая процедура: Высокосортный пирит подвергали сухому измельчению для прохождения через сито 150 меш. Двадцатиграммовые порции пирита переносили в делительные воронки на 400 мл. щелочного раствора. Воздух с постоянной скоростью пропускали вверх по стволам воронок. Образцы пульпы отбирали через различные промежутки времени, фильтровали и анализировали. Один раствор с рН 10,8 в начале, снизился до рН 3,2 после 30 часов аэрации; рН другого раствора снизился с 12,1 до 8,5 за тот же период. Установлено, что продуктами реакции воздуха на щелочную пиритную пульпу являются сульфид, тиосульфат, сульфит, сульфат и небольшое количество свободной серы. В исходном растворе с рН 12,1 было обнаружено гораздо больше сульфида, чем в растворе, исходном с рН 10,8. Содержание сульфидов и сульфитов в обоих растворах уменьшалось по мере снижения щелочности. Содержание сульфата, тиосульфата и общего содержания серы постепенно увеличивалось со временем.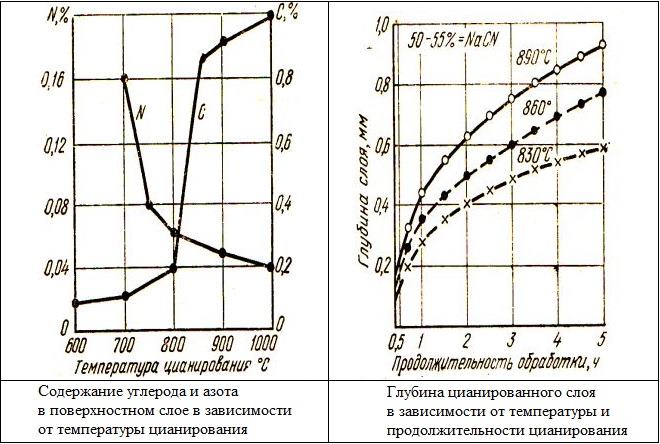
Сульфид окисляется, в то время как гидроксильные ионы остаются или адсорбируются на поверхности, тем самым подавляя любую дальнейшую реакцию. Однако, если контур станет слишком кислым, поверхностные гидроксильные ионы будут удалены, а новые поверхности подвергнутся дальнейшему разложению.
Были проведены дальнейшие эксперименты, в которых изучалось действие цианида на пирит; процедура аналогична описанной ранее. Предварительные испытания, проведенные в отсутствие пирита, показали, что тиосульфат натрия и цианид натрия в присутствии воздуха очень медленно реагируют с образованием тиоцианата; в аналогичных условиях сера и цианид реагируют гораздо быстрее с образованием тиоцианата. В отсутствие воздуха сульфид натрия и цианид очень медленно реагируют с образованием тиоцианата; в присутствии воздуха эта реакция протекает намного быстрее, но медленнее, чем реакция между серой и цианидом. В присутствии пирита образование тиоцианата шло непрерывно. Однако это составляло лишь около одной трети общих потерь цианида. Считалось, что по крайней мере часть оставшихся потерь вызвана фиксацией цианида на пирите. Кондиционирование пирита в щелочном растворе привело к заметному снижению количества теряемого цианида.
Считалось, что по крайней мере часть оставшихся потерь вызвана фиксацией цианида на пирите. Кондиционирование пирита в щелочном растворе привело к заметному снижению количества теряемого цианида.
ПРИМЕР Практика цианирования описана при обработке руды с высоким содержанием пирротина, которая по существу представляет собой сложную кварцевую, карбонатную, сульфидную руду, имеющую следующий приблизительный состав: SiO, 19,6%; Fe 32,2%; С 14,6%; Как 3,5%; Al2O3 0,4%; МпО 0,9%; СаО 2,4%; MgO 7,6%.; Cu 0,1%.; CO, 15,7%% Au 0,60 унций/т. Он состоит из тонкокристаллической примеси кварца, кальцита, доломита, сидерита, анкерита, пирротина, пирита и арсенопирита как основных минералов с небольшими количествами халькопирита и хлорита; пирротин является преобладающим сульфидом. Золото чаще всего связано с арсенопиритом в контакте с пирротином. Общее правило состоит в том, что руда с высоким содержанием мышьяка богата золотом, а руда с высоким содержанием пирротина относительно бедна.
При обработке этой руды продукт с высоким содержанием золота концентрируется на столах и пластах; этот концентрат обрабатывается отдельно для извлечения золота. Хвосты пласта с добавлением 0,5 фунта извести на тонну измельчаются и разделяются на пески и шламы, которые цианируются отдельно. Растворы цианирования богаты ферроцианидом и тиоцианатом из-за пирротина. Если растворы повторно использовать для дальнейшего растворения золота и серебра, эти примеси накапливаются в растворе так быстро, до таких высоких процентов, что осаждение ценностей становится не только проблемой, но и почти невозможным. Следовательно, объемы раствора должны быть низкими, а цианирование толстой пульпы должно быть возвращено. Бесплодные решения отбрасываются.
Каждую порцию песка или шлама перемешивают и аэрируют в течение 12 часов, когда раствор золота достигает равновесия. Начиная со 100 гран (0,208 унции) на тонну, проба песка снижается до 25–30 гран (0,052–0,063 унции) на тонну, после чего дальнейшее взбалтывание дает лишь немного увеличенный раствор золота. Длительное перемешивание нецелесообразно, так как концентрация цианистого раствора быстро падает и может произойти переосаждение золота. Начиная с примерно 0,25% NaCN для песков или шламов, сила цианида падает примерно до 0,08% NaCN для песчаных загрузок и 0,02% NaCN для чистых шламовых загрузок с примерно равным извлечением золота в каждом случае. Следовательно, перепроизводство шлама увеличивает потребление цианида. Около 0,5 фунта твердой извести на тонну песка добавляют вместе с цианидом. Добавление от 3 до 4 фунтов. извести на тонну поддерживает более высокую цианидную прочность, но повышает содержание хвостов до 50 гран (0,104 унции) на тонну. Наилучшие результаты получаются при низкой щелочности, добавление большого количества извести приводит только к образованию полисульфидов кальция. Частичный анализ типичного обогащенного раствора, помещаемого в цинковые ящики, показывает, что он содержит 0,012 % свободного NaCN, отсутствие защитной щелочности, 0,182 % Na4Fe(CN)6, следы Na3Fe(CN)6, 0,066 % NaCNS, 0,005 % меди.
Длительное перемешивание нецелесообразно, так как концентрация цианистого раствора быстро падает и может произойти переосаждение золота. Начиная с примерно 0,25% NaCN для песков или шламов, сила цианида падает примерно до 0,08% NaCN для песчаных загрузок и 0,02% NaCN для чистых шламовых загрузок с примерно равным извлечением золота в каждом случае. Следовательно, перепроизводство шлама увеличивает потребление цианида. Около 0,5 фунта твердой извести на тонну песка добавляют вместе с цианидом. Добавление от 3 до 4 фунтов. извести на тонну поддерживает более высокую цианидную прочность, но повышает содержание хвостов до 50 гран (0,104 унции) на тонну. Наилучшие результаты получаются при низкой щелочности, добавление большого количества извести приводит только к образованию полисульфидов кальция. Частичный анализ типичного обогащенного раствора, помещаемого в цинковые ящики, показывает, что он содержит 0,012 % свободного NaCN, отсутствие защитной щелочности, 0,182 % Na4Fe(CN)6, следы Na3Fe(CN)6, 0,066 % NaCNS, 0,005 % меди. , 0,0005% мышьяка.
, 0,0005% мышьяка.
Описаны дальнейшие разработки цианирования в направлении контроля щелочности, поскольку было известно, что избыток извести в цианидной пульпе вреден. Для максимального извлечения золота оптимальная потребность в извести была небольшой. Обычный метод для титрования щелочности оказался сомнительным, когда щелочность была очень низкой, особенно в присутствии некоторых растворенных солей, обладающих буферными свойствами. Поэтому в качестве меры щелочности использовали обозначение pH. Установлено, что при цианировании пульпы высокой плотности оптимальное значение рН раствора лежит в пределах 8-9.. При однократном использовании растворов оказалось затруднительным поддерживать рН в этих пределах. Бесплодное решение было найдено гораздо лучше в этом отношении. При уровне щелочи выше pH 10 потребление цианида и растворение золота уменьшались; цианидная деструкция тяготела скорее к образованию тиоцианатов, что, по-видимому, подтверждало гипотезу о воздействии избытка щелочи на пирротин.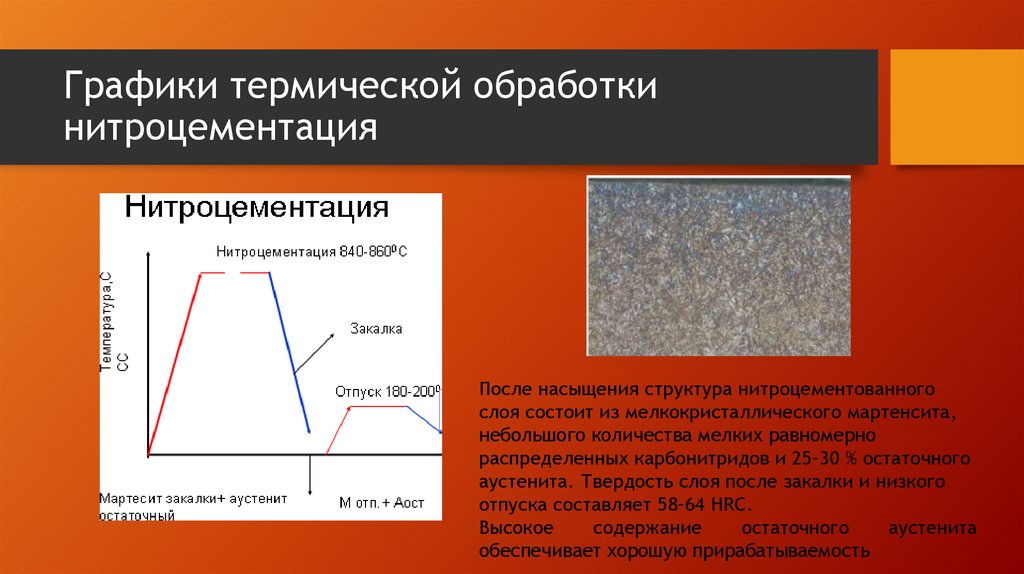 Ниже рН 7 разрушение цианидов было очень сильным, с тенденцией скорее к образованию ферроцианидов и выделению газообразного HCN.
Ниже рН 7 разрушение цианидов было очень сильным, с тенденцией скорее к образованию ферроцианидов и выделению газообразного HCN.
Было исследовано использование различных солей металлов. Соли кадмия и цинка модифицировали потребление цианидов, по-видимому, подавляя образование ферроцианидов, в то время как соли свинца и ртути, помимо снижения потребления цианидов, позволяли увеличить извлечение золота. В расчете на единицу массы реагента соли ртути были более активны, чем соли ртути, в то время как обе они были более активны, чем свинец. Среди протестированных солей свинца растворимые соли были более активны для того же веса металла, чем относительно нерастворимые оксиды. По мере увеличения количества свинца относительная доля тиоцианата по сравнению с ферроцианидом в конечном растворе увеличивалась, а общее потребление цианида снижалось. В присутствии свинца рН раствора цианида в начале был 90,6, снижаясь до pH 8, когда достигается максимальное извлечение золота.
При оптимальном количестве свинца и других реагентов скорость растворения золота была примерно пропорциональна количеству нагнетаемого воздуха. Однако высокая стоимость и нестабильные условия рН, вызванные интенсивной аэрацией пульпы, перевешивают преимущества повышенной скорости растворения золота.
Однако высокая стоимость и нестабильные условия рН, вызванные интенсивной аэрацией пульпы, перевешивают преимущества повышенной скорости растворения золота.
В результате вышеуказанных выводов практика цианирования была изменена следующим образом: Рудная пульпа, состоящая как из песка, так и из шлама, подается в секцию цианирования в виде густой вязкой пульпы, содержащей около 65 или 70% твердых веществ. При спуске в мешалки добавляют взвесь твердой извести в воде. Для загрузки песка требуется от 0,7 до 1,1 фунта извести на тонну твердого вещества, а для загрузки шлама от 2 до 3 фунтов. за тонну. По-видимому, чем меньше размер частиц, т.е. чем больше площадь поверхности, тем больше требуется извести для пульпы. Густую мезгу перемешивают и кратковременно аэрируют. рН раствора во время этого предварительного кондиционирования составляет от 10,0 до 10,4. Затем к пульпе добавляют пустой раствор, чтобы разбавить ее до 50% твердых веществ. При этом добавляют около 1 фунта соли свинца на тонну твердых веществ, растворенных в воде. Щелочность раствора теперь равна pH 9..6 до 9.8, и представляется важным, чтобы этот верхний предел не превышался. Свежий раствор цианида натрия добавляют к пульпе, чтобы повысить содержание свободного цианида в растворе до 0,07% NaCN. Пульпу перемешивают в течение 6 часов*. В конце этого периода pH раствора составляет около 8. Пульпу фильтруют после добавления небольшого количества извести для облегчения фильтрации. Осаждение золота проводят в цинковых ящиках. Настоящий способ обработки извлекает около 80% золота из сырья для цианирования; это снизило анализ основного хвоста примерно на 50%.
Щелочность раствора теперь равна pH 9..6 до 9.8, и представляется важным, чтобы этот верхний предел не превышался. Свежий раствор цианида натрия добавляют к пульпе, чтобы повысить содержание свободного цианида в растворе до 0,07% NaCN. Пульпу перемешивают в течение 6 часов*. В конце этого периода pH раствора составляет около 8. Пульпу фильтруют после добавления небольшого количества извести для облегчения фильтрации. Осаждение золота проводят в цинковых ящиках. Настоящий способ обработки извлекает около 80% золота из сырья для цианирования; это снизило анализ основного хвоста примерно на 50%.
Реакционная способность сульфидных минералов и ее влияние на растворение золота и его электрохимическое поведение в цианиде
Образцы различных пород, добытых на руднике, измельчали и цианировали в закрытых бутылях с 0,1% раствором NaCN. Известно, что образец, содержащий много анкерита, СаСО3(Mg, Fe, Mn)СО3, почти свободный от сульфидов, потреблял много цианида, образуя исключительно ферроцианид.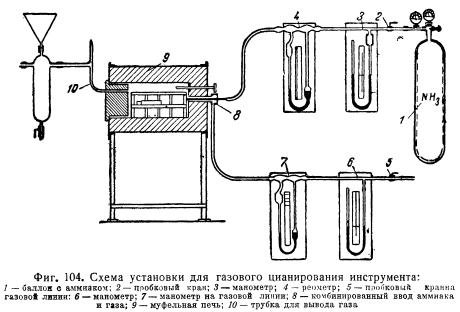 Заметной реакции между сидеритом и цианидом не наблюдалось при поддержании рН раствора выше 7,9.0008
Заметной реакции между сидеритом и цианидом не наблюдалось при поддержании рН раствора выше 7,9.0008
Цианидный процесс | металлургия | Британика
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- В этот день в истории
- Викторины
- Подкасты
- Словарь
- Биографии
- Резюме
- Популярные вопросы
- Инфографика
- Демистификация
- Списки
- #WTFact
- Товарищи
- Галереи изображений
- Прожектор
- Форум
- Один хороший факт
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- Britannica объясняет
В этих видеороликах Britannica объясняет различные темы и отвечает на часто задаваемые вопросы.
- Britannica Classics
Посмотрите эти ретро-видео из архивов Encyclopedia Britannica. - Demystified Videos
В Demystified у Britannica есть все ответы на ваши животрепещущие вопросы. - #WTFact Видео
В #WTFact Britannica делится некоторыми из самых странных фактов, которые мы можем найти. - На этот раз в истории
В этих видеороликах узнайте, что произошло в этом месяце (или любом другом месяце!) в истории.
- Студенческий портал
Britannica — это лучший ресурс для учащихся по ключевым школьным предметам, таким как история, государственное управление, литература и т. д. - Портал COVID-19
Хотя этот глобальный кризис в области здравоохранения продолжает развиваться, может быть полезно обратиться к прошлым пандемиям, чтобы лучше понять, как реагировать сегодня. - 100 женщин
Britannica празднует столетие Девятнадцатой поправки, выделяя суфражисток и политиков, творящих историю.


