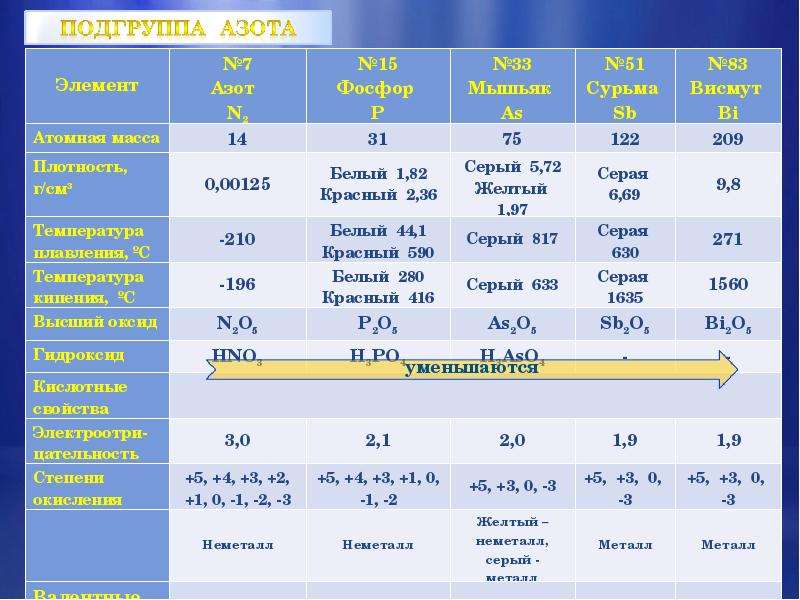
Содержание
ICSC 0775 — СУРЬМА
ICSC 0775 — СУРЬМА
« back to the search result list(ru)
Chinese — ZHEnglish — ENFinnish — FIFrench — FRGerman — DEHebrew — HEHungarian — HUItalian — ITJapanese — JAKorean — KOPersian — FAPolish — PLPortuguese — PTRussian — RUSpanish — ES
| СУРЬМА | ICSC: 0775 (Октябрь 2006) |
| CAS #: 7440-36-0 |
| UN #: 2871 |
| EINECS #: 231-146-5 |
| ОСОБЫЕ ОПАСНОСТИ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ТУШЕНИЕ ПОЖАРА | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Горючее при определенных условиях. При пожаре выделяет раздражающие или токсичные пары (или газы). Мелкодисперсные частицы образуют в воздухе взрывчатые смеси. Риск взрыва при контакте с кислотами или галогенами. При пожаре выделяет раздражающие или токсичные пары (или газы). Мелкодисперсные частицы образуют в воздухе взрывчатые смеси. Риск взрыва при контакте с кислотами или галогенами. | НЕ использовать открытый огонь. НЕ допускать контакта с окислителями, галогеном или кислотами. Замкнутая система, взрывозащищенное (для пыльной среды) электрическое оборудование и освещение. Не допускать оседания пыли. | Использовать распыленную воду, пену, порошок, двуокись углерода. |
| НЕ ДОПУСКАТЬ ОБРАЗОВАНИЕ ПЫЛИ! | |||
|---|---|---|---|
| СИМПТОМЫ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ПЕРВАЯ ПОМОЩЬ | |
| Вдыхание | Кашель. См. проглатывание. | Применять местную вытяжку или средства защиты органов дыхания. | Свежий воздух, покой. |
| Кожа | Защитные перчатки. | Снять загрязненную одежду. Ополоснуть и затем промыть кожу водой с мылом. | |
| Глаза | Покраснение. Боль. | Использовать закрытые защитные очки или средства защиты глаз в комбинации со средствами защиты органов дыхания если вещество в порошкообразном соостоянии. | Прежде всего промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно сделать без затруднений), затем обратится за медицинской помощью. |
| Проглатывание | Боль в животе. Рвота. Диарея. | Не принимать пищу, напитки и не курить во время работы. | Прополоскать рот. Обратиться за медицинской помощью . |
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
Индивидуальная защита: Респиратор с сажевым фильтром, подходящий для концентрации вещества в воздухе. БлокируемыеСмести просыпанное вещество в закрытые контейнеры. При необходимости, сначала намочить, чтобы избежать появления пыли. БлокируемыеСмести просыпанное вещество в закрытые контейнеры. При необходимости, сначала намочить, чтобы избежать появления пыли. | Согласно критериям СГС ООН
Транспортировка |
| ХРАНЕНИЕ | |
| Отдельно от окислителей, кислот, галогенов и пищевых продуктов и кормов. | |
| УПАКОВКА | |
| Не перевозить с продуктами питания и кормами для животных. |
| СУРЬМА | ICSC: 0775 |
| ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА | |
|---|---|
Агрегатное Состояние; Внешний Вид Физические опасности Химические опасности | Формула: Sb |
| ВОЗДЕЙСТВИЕ НА ОРГАНИЗМ И ЭФФЕКТЫ ОТ ВОЗДЕЙСТВИЯ | |
|---|---|
Пути воздействия Эффекты от кратковременного воздействия | Риск вдыхания Эффекты от длительного или повторяющегося воздействия |
| Предельно-допустимые концентрации |
|---|
| TLV: 0.5 mg/m3, как TWA. MAK: (включая его неорганические соединения, кроме сурьмы): канцерогенная категория: 2; мутагенная группа зародышевых клеток: 3A |
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
| ПРИМЕЧАНИЯ |
|---|
Other boiling points: 1325°C, 1440°C, 1587 °C, 1750°C.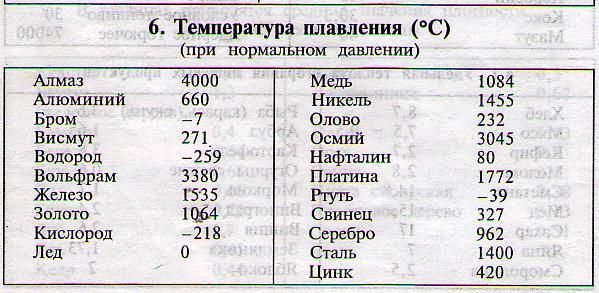 The recommendations on this card apply only to metallic antimony. См. карты ICSC 0012, 0220, 0776 и 1224. |
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
| Классификация ЕС |
| (ru) | Ни МОТ, ни ВОЗ, ни Европейский Союз не несут ответственности за качество и точность перевода или за возможное использование данной информации. © Версия на русском языке, 2018 |
Сурьма — что это за металл
Сурьма металлическая — 51-й химический элемент в периодической таблице Менделеева, обозначается символом Sb. Это полуметалл с зернистым строением и светлым голубовато-серебристым оттенком. В свободном состоянии представляет собой кристаллы с металлическим блеском.
Сурьма как вещество: физические свойства
Внешне вещество похоже на металл, однако характеризуется меньшей электро- и теплопроводностью. Оно отличается хрупкостью (легко растирается в порошок) и способностью расширяться при застывании.
Оно отличается хрупкостью (легко растирается в порошок) и способностью расширяться при застывании.
Элемент существует в четырех модификациях:
- Кристаллическая, или серая (основная модификация).
- Черная (аморфная).
- Взрывчатая (аморфная).
- Желтая (аморфная).
Кристаллическая сурьма
В основной модификации полуметалл образует игольчатые кристаллы в форме звезд. Чем меньше примесей, тем толще кристаллы. Вещество начинает плавиться при температуре +630,5 ⁰C, закипает — при +1634 ⁰C. Обладает диамагнитностью, т.е. намагничивается против направления внутреннего поля.
Основные свойства вещества:
- Плотность при стандартных условиях — 6,691 г/см3.
- Удельная теплоемкость — 0,210 кДж/(кг*К) при температурах от 20 ⁰С до 200 ⁰С.
- Молярная теплоемкость — 25,2 Дж/(K*моль).
- Теплопроводность — 17,6 вт/(м*К) при температуре 20 ⁰C.

- Молярный объем — 18,4 см3/моль.
- Удельная теплота плавления — 20,08 кДж/моль.
- Удельная теплота испарения — 195,2 кДж/моль.
В основной модификации металл устойчив при стандартных условиях. Он имеет слоистую структуру.
Черная сурьма
Это аморфная металлическая модификация, которая образуется из кристаллической сурьмы при резком охлаждении паров вещества. Она имеет плотность 5,3 г/см3. Данная неустойчивая модификация в безвоздушном пространстве при нагреве до 400 ⁰С переходит в кристаллическую сурьму.
Желтая сурьма
Чтобы получилась желтая сурьма, требуется воздействие кислорода на сниженный стибин Sbh4. Эта модификация содержит небольшой процент химически связанного водорода. Является неустойчивой: переходит в черную сурьму при освещении или нагревании.
Взрывчатая сурьма
Электролиз раствора SbCl3 в соляно-кислой среде приводит к образованию взрывчатой сурьмы. Она имеет плотность от 5,64 до 5,97 г/см3, внешне напоминает графит. При любом прикосновении взрывается и превращается в кристаллическую сурьму.
Она имеет плотность от 5,64 до 5,97 г/см3, внешне напоминает графит. При любом прикосновении взрывается и превращается в кристаллическую сурьму.
Сурьма и человек: историческая справка
Этот металл применялся с доисторических времен. При раскопках на территории древнего Вавилона археологи обнаружили сосуды из металлической сурьмы. Изделия датируются 3 тысячелетием до н.э.
Предметы из этого металла также были найдены в Грузии: находки относятся к 1 тысячелетию до н.э. В древности металл использовался в сплаве со свинцом, медью или оловом.
С XIX в. до н.э. в Древнем Египте и странах Азии (Индия, Междуречье и др.) повсеместно применялся «сурьмяный блеск» — черный порошок из соединений полуметалла, который использовался для грима (в основном для чернения бровей).
До конца неизвестно происхождение самого названия. В тюркских языках существует слово surme, которое обозначает «грим, мазь». В персидском «сурме» значит «металл».
Сурьма и организм: несколько слов о биологии
Сурьма относится к макроэлементам и участвует в обменных процессах многих живых организмов. Среднее количество элемента в растениях — 0, 06 мг, в наземных животных — 0,0006 мг, в морских животных — 0,02 мг. В организме человека содержится не более 0,00001% сурьмы по массе. Она поступает с воздухом, пищей и водой, содержится в щитовидной железе, эритроцитах и плазме крови, печени, почках, костной ткани, селезенке. В среднем за сутки поступает около 50 мкг и выводится мочой и фекалиями.
Среднее количество элемента в растениях — 0, 06 мг, в наземных животных — 0,0006 мг, в морских животных — 0,02 мг. В организме человека содержится не более 0,00001% сурьмы по массе. Она поступает с воздухом, пищей и водой, содержится в щитовидной железе, эритроцитах и плазме крови, печени, почках, костной ткани, селезенке. В среднем за сутки поступает около 50 мкг и выводится мочой и фекалиями.
До конца не изучены физиологическая и биохимическая функции макроэлемента, поэтому нет достоверных данных о возможных последствиях ее дефицита в организме. При этом установлено, что избыток вещества препятствует белковому, жировому и углеводному обменам. Если сурьма накапливается в щитовидной железе, она угнетает ее работу и вызывает эндемический зоб. При одноразовом попадании в пищеварительный тракт вызывает рефлекторную рвоту и полностью выводится. При регулярных поступлениях избыточного количество сурьмы в пищевод возможны заболевания желудочно-кишечного тракта, в том числе язвы.
Токсичные пары металла могут вызвать поражения кожи и носовые кровотечения. В зоне риска — люди, которые работают с этим металлом постоянно: печатники, эмалировщики и др.
В зоне риска — люди, которые работают с этим металлом постоянно: печатники, эмалировщики и др.
В малых дозах макроэлемент применяется в медицине — в основном, в составе отхаркивающих и рвотных средств.
Сурьма как элемент: химические свойства
Металлическая сурьма малоактивна и устойчива на открытом воздухе при нормальных температурах. Начинает окислятся при +630 ⁰С, в результате чего образуется соединение Sb2O3 — оксид сурьмы. Полуметалл не вступает в реакции с водородом, азотом, кремнием и бором, остается устойчивым к воде, а в расплавленном виде незначительно растворяет углерод.
В результате возможных химических реакций образуются следующие вещества:
- Сульфид сурьмы — при сплавлении с серой.
- Интерметаллические соединения (антимониды) — при взаимодействии с мышьяком, медью, палладием и некоторыми другими металлами.
- Хлорид сурьмы — при растворении в хлоре.
- Сульфат сурьмы — при растворении в соляной кислоте.

- Сурьмяная кислота — в результате реакции с концентрированной азотной кислотой.
Полуметалл растворяется в «царской водке» — смеси винной и азотной кислот.
Сурьма как полезное ископаемое: добыча и производство
Месторождения металлической сурьмы находятся в ЮАР, Китае, Алжире, России, Болгарии, Азербайджане, Киргизии, Сербии, Финляндии, Казахстане, Таджикистане. Содержание элемента в земной коре невелико — 500 мг/т. Большая часть вещества сконцентрирована в осадочных породах — бокситах, фосфоритах, глинистых сланцах. Меньше всего ископаемого содержится в песчаниках и известняках.
Более 70% этого металла производится в Китае, а остальные 30% делят Россия, Мьянма, Боливия, Таджикистан, ЮАР, Канада, Австралия и некоторые другие страны.
На территории Китая также находятся самые крупные резервы — более 50% мировых запасов. Около 20% расположено в России, 16% — в Боливии, 3% — в Таджикистане, 1% — в ЮАР, менее 10% рассредоточено по разным странам.
Сурьма как ресурс: применение
Металлургия
Поскольку сурьма — хрупкий металл, в металлургической промышленности она практически не применяется отдельно. Зато в сплавах она повышает прочность других металлов и препятствует окислению.
Сплав сурьмы, олова и свинца называется «гарт» (в переводе с украинского — «зеркала»). Он на протяжении многих веков используется в типографии для изготовления шрифтов. В основу положено свойство сурьмы расширяться при затвердевании: благодаря этому сплав более плотно заполняет литейную матрицу. Помимо этого, сурьма повышает износостойкость шрифта. Гарт также используется для отливки пуль, изготовления кабелей, труб для протока агрессивных жидкостей и др.
Сплав свинца и сурьмы отличается твердостью и устойчивостью к коррозии. Он применяется в химическом машиностроении.
Баббиты (подшипниковые сплавы) широко используются в железнодорожном, автомобильном транспорте и станкостроении. Они содержат сурьму, олово, медь и свинец. Имеют высокую твердость, стойкость к истиранию и коррозии.
Имеют высокую твердость, стойкость к истиранию и коррозии.
Всего существует порядка 200 сплавов различных металлов с сурьмой. В том числе она добавляется к металлам для хрупкой отливки.
Полупроводниковая промышленность
Полуметалл входит в свинцовые сплавы, используется при производстве диодов, ИК детекторов, датчиков Холла и других элементов в полупроводниковой промышленности.
Медицина
Стибнит, природный сульфит сурьмы, в древности применялся в качестве лекарства от паразитов. В некоторых странах его до сих пор добавляют в препараты. Соединения металла применяются для лечения лейшманиозов и глазных заболеваний.
Другие области применения
Оксид сурьмы используют в текстильной промышленности как закрепитель. Он также входит в состав многих эмалей и красок. Пятиокись металла применяется при изготовлении стекла, люминесцентных ламп, резины. Трехсернистая сурьма входит в состав спичек. Металла находит применение в электронике (для некоторых припоев) и в термоэлектрический сплавах.
Сурьма — Температура плавления — Температура кипения
Автор
Сурьма — Температура плавления и кипения
Температура плавления сурьмы 63 1°С .
Температура кипения сурьмы: 1950°C .
Обратите внимание, что эти точки связаны со стандартным атмосферным давлением.
Температура кипения – насыщение
В термодинамике, насыщение определяет состояние, при котором смесь пара и жидкости может существовать вместе при заданной температуре и давлении. Температура, при которой начинает происходить испарение (кипение) при данном давлении, называется температурой насыщения или точкой кипения . Давление, при котором начинается испарение (кипение) при данной температуре, называется давлением насыщения. Когда ее рассматривают как температуру обратного перехода из пара в жидкость, ее называют точкой конденсации.
Когда ее рассматривают как температуру обратного перехода из пара в жидкость, ее называют точкой конденсации.
Точка плавления
В термодинамике точка плавления определяет состояние, при котором твердое тело и жидкость могут существовать в равновесии. Добавление тепла превратит твердое вещество в жидкость без изменения температуры. Температура плавления вещества зависит от давления и обычно указывается при стандартном давлении. Когда ее рассматривают как температуру обратного перехода от жидкого к твердому, ее называют точкой замерзания или точкой кристаллизации.
Первая теория, объясняющая механизм плавления в объеме, была предложена Линдеманном, который использовал колебание атомов в кристалле для объяснения плавления. Твердые тела похожи на жидкости тем, что оба находятся в конденсированном состоянии, а частицы находятся гораздо ближе друг к другу, чем частицы газа. Атомы в твердом теле тесно связаны друг с другом либо в правильной геометрической решетке (кристаллические твердые тела, которые включают металлы и обычный лед), либо в неправильной (аморфное твердое тело, такое как обычное оконное стекло), и обычно имеют низкую энергию. движение отдельных атомов , ионов или молекул в твердом теле ограничено колебательным движением вокруг фиксированной точки. Когда твердое тело нагревается, его частицы вибрируют быстрее , поскольку твердое тело поглощает кинетическую энергию. В какой-то момент амплитуда колебаний становится настолько большой, что атомы начинают вторгаться в пространство своих ближайших соседей и возмущать их, и начинается процесс плавления. Точка плавления – это температура, при которой разрушающие вибрации частиц твердого тела преодолевают силы притяжения, действующие внутри твердого тела.
движение отдельных атомов , ионов или молекул в твердом теле ограничено колебательным движением вокруг фиксированной точки. Когда твердое тело нагревается, его частицы вибрируют быстрее , поскольку твердое тело поглощает кинетическую энергию. В какой-то момент амплитуда колебаний становится настолько большой, что атомы начинают вторгаться в пространство своих ближайших соседей и возмущать их, и начинается процесс плавления. Точка плавления – это температура, при которой разрушающие вибрации частиц твердого тела преодолевают силы притяжения, действующие внутри твердого тела.
Сурьма – свойства
| Элемент | Сурьма |
|---|---|
| Атомный номер 9 0071 | 51 |
| Символ | Sb |
| Категория элемента | Металлоиды |
| Фаза при STP | Твердое тело |
Атомная масса [а. е.м.] е.м.] | 121,76 |
| Плотность при STP [г/см3] | 6,697 |
| Электронная конфигурация | [Kr] 4d10 5s2 5p3 |
| Возможные степени окисления | +3,5/-3 |
| Сродство к электрону [кДж/моль] | 103,2 |
| Электроотрицательность [ Полинга] | 2,05 |
| 1-я энергия ионизации [эВ] | 8,64 |
| Год открытия | неизвестно |
| Первооткрыватель | неизвестно |
| Термические свойства | |
| Температура плавления [шкала Цельсия] | 631 |
| Температура кипения [шкала Цельсия] | |
| Теплопроводность [Вт/м·К] | 24 |
| Удельная теплоемкость [Дж/г·К] | 0,21 |
| Теплота плавления [кДж/моль] | 19,87 |
| Теплота парообразования [кДж/моль] моль] | 77,14 |
| Водород1H | Гелий2Не | ||||||||||||||||||
| Литий3Li | Бериллий4Be | Бор5B | Углерод6C | Азот7N | Кислород8O | Фтор9F | Неон10Ne | ||||||||||||
| Натрий-11Na | Магний-12Mg | Алюминий13Al | Кремний14Si | Фосфор15P | Сера16S | Хлор17Cl | Аргон18Ar | ||||||||||||
| Калий19K | Кальций20Ca | Скандий21Sc | Титан22Ti 900 71 | Ванадий23V | Хром24Cr | Марганец25Mn | Железо26Fe | Кобальт27Co | Никель28Ni | Медь29Cu 90 071 | Цинк30Zn | Галлий31Ga | Германий32Ge | Мышьяк33As | Селен34Se | Бром35Br | Криптон36Kr | ||
| Рубидий37Rb | Стронций38Sr | Иттрий39Y | Цирконий40Zr | Ниоб ium41Nb | Молибден42Mo | Технеций43Tc | Рутений44Ru | Родий45Rh | Палладий46Pd | Silver47Ag 90 071 | Кадмий48Cd | Индий49In | Олово50Sn | Сурьма51Sb | Теллур52Te | Йод53I | Ксенон54Xe | ||
| Цезий55Cs | Барий56Ba | Лантан57La | Гафний72Hf | Тантал73Ta | Вольфрам74W | Рений75Re | Осмий76Os | Иридий77Ir | Платина78Pt | Золото79Au | Ртуть80Hg | Таллий81Tl | Свинец82Pb | Висмут83Bi | Полоний84Po | Астатин85At | Радон86Rn | ||
| Francium87Fr | Radium88Ra | Actinium89Ac | Rutherfordium104Rf | Dubnium105Db | Seaborgium 106Sg | Bohrium107Bh | Hassium108Hs | Meitnerium109Mt | Darmstadtium110Ds | Roentgenium111Rg | Co pernicium112Cn | Nihonium113Nh | Flerovium114Fl | Moscovium115Mc | Livermorium116Lv | Теннесси117Ц | Oganesson118Og | ||
| Cerium58Ce | Празеодим5 9Pr | Неодим60Nd | Прометий61Pm | Самарий62Sm | Европий63Eu | Гадолиний64Gd | Тербий65Tb 900 71 | Dysprosium66Dy | Holmium67Ho | Erbium68Er | Thulium69Tm | Иттербий70Yb | Лютеций71Lu | ||||||
| Торий90Th | Протактиний91Pa | Уран92U | Нептуний93Np | Plutonium94Pu | Americium95Am | Curium96Cm | Berkelium97Bk | Californianium98Cf | Einsteinium99Es | Fermium100 Fm | Mendelevium101Md | Nobelium102No | Lawrencium103Lr | ||||||
–
–
–
сообщите об этом объявлении
Общая информация о сурьме
ПОЛЕЗНЫЕ ССЫЛКИ ДЛЯ Sb | ||||||
PSA — информация о сурьме www. www.wikipedia.org www.environmentalchemistry.com http://www.atsdr.cdc.gov | ||||||
Быстрый |
Название элемента: сурьма |
Что | ||
Сурьма используется для повышения твердости сплавов со свинцовыми сплавами для аккумуляторов, со сплавами свинца/меди/олова для подшипников машин. Он также используется в автомобильных сцеплениях и тормозных деталях. Другим основным применением является трехокись сурьмы, которая используется для производства огнезащитных химикатов. Сурьма используется в полупроводниковой промышленности для производства некоторых силиконовых пластин, диодов и инфракрасных детекторов. Небольшие количества используются в производстве безопасных спичек. Как | ||






 webelements.com
webelements.com