Содержание
Коррозия металлов и способы защиты от нее
| Коррозия – это процесс разрушения металлов и металлических конструкций под воздействием различных факторов окружающей среды – кислорода, влаги, вредных примесей в воздухе. |
Коррозионная стойкость металла зависит от его природы, характера среды и температуры.
- Благородные металлы не подвергаются коррозии из-за химической инертности.
- Металлы Al, Ti, Zn, Cr, Ni имеют плотные газонепроницаемые оксидные плёнки, которые препятствуют коррозии.
- Металлы с рыхлой оксидной плёнкой – Fe, Cu и другие – коррозионно неустойчивы. Особенно сильно ржавеет железо.
Различают химическую и электрохимическую коррозию.
Химическая коррозия сопровождается химическими реакциями. Как правило, химическая коррозия металлов происходит при действии на металл сухих газов, её также называют газовой. |
3Fe + 2O2 = Fe3O4
При химической коррозии также возможны процессы:
Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3
Как правило, такие процессы протекают в аппаратах химических производств.
| Электрохимическая коррозия – это процесс разрушения металла, который сопровождается электрохимическими процессами. Как правило, электрохимическая коррозия протекает в присутствии воды и кислорода, либо в растворах электролитов. |
В таких растворах на поверхности металла возникают процессы переноса электронов от металла к окислителю, которым является либо кислород, либо кислота, содержащаяся в растворе.
При этом электродами являются сам металл (например, железо) и содержащиеся в нем примеси (обычно менее активные металлы, например, олово).
В таком загрязнённом металле идёт перенос электронов от железа к олову, при этом железо (анод) растворяется, т.е. подвергается коррозии:
Fe –2e = Fe 2+
На поверхности олова (катод) идёт процесс восстановления водорода из воды или растворённого кислорода:
2H+ + 2e → H2
O2 + 2H2O + 4e → 4OH–
| Например, при контакте железа с оловом в растворе соляной кислоты происходят процессы: |
Анод: Fe –2e → Fe 2+
Катод: 2H+ + 2e → H2
Суммарная реакция: Fe + 2H+ → H2 + Fe2+
Если реакция проходит в атмосферных условиях в воде, в ней участвует кислород и происходят процессы:
Анод: Fe –2e → Fe 2+
Катод: O2 + 2H2O + 4e → 4OH–
Суммарная реакция:
Fe 2+ + 2OH – → Fe(OH)2
4Fe(OH)2 + O2+ 2H2O → 4Fe(OH)3
При этом образуется ржавчина.
Защитные покрытия
Защитные покрытия предотвращают контакт поверхности металла с окислителями.
- Катодное покрытие – покрытие менее активным металлом (защищает металл только неповреждённое покрытие).
- Покрытие краской, лаками, смазками.
- Создание на поверхности некоторых металлов прочной оксидной плёнки химическим путём (анодирование алюминия, кипячение железа в фосфорной кислоте).
Создание сплавов, стойких к коррозии
Физические свойства сплавов могут существенно отличаться от свойств чистых металлов. Добавление некоторых металлов может приводить к повышению коррозионной стойкости сплава. Например, нержавеющая сталь, новые сплавы с большой коррозионной устойчивостью.
Изменение состава среды
Коррозия замедляется при добавлении в среду, окружающую металлическую конструкцию, ингибиторов коррозии. Ингибиторы коррозии — это вещества, подавляющие процессы коррозии.
Электрохимические методы защиты
Протекторная защита: при присоединении к металлической конструкции пластинок из более активного металла – протектора. В результате идёт разрушение протектора, а металлическая конструкция при этом не разрушается.
Понравилось это:
Нравится Загрузка…
Коррозия металла – виды и способы защиты – рекомендации от ТК Газметаллпроект
Коррозийные процессы представляют наиболее реальную угрозу для металлических конструкций. Вне зависимости от толщины стали, ржавчина способна быстро привести материал в негодность. В некоторых случаях, при небольших повреждениях, развитие коррозии удается остановить, а последствия ликвидировать. Чаще всего приходится менять металлические элементы полностью. Поэтому защита стали от коррозии является первоочередной задачей при строительстве и эксплуатации конструкций.
Причины и последствия образования коррозии на металле
В идеальных условиях любой металл сохраняет свои характеристики в течение длительного периода времени. Даже если в состав материала не входят дополнительные примеси, отсутствие внешних воздействий позволяет сохранять прочность и жесткость конструкции. В реальной жизни таких условий добиться практически невозможно. Коррозийные процессы могут быть вызваны следующими причинами:
Даже если в состав материала не входят дополнительные примеси, отсутствие внешних воздействий позволяет сохранять прочность и жесткость конструкции. В реальной жизни таких условий добиться практически невозможно. Коррозийные процессы могут быть вызваны следующими причинами:
- повышенная влажность воздуха, за счет которой металл постоянно подвергается значительным нагрузкам и очень быстро начинает окисляться;
- выпадение осадков на незащищенную поверхность стали также влечет за собой распространение очагов коррозии;
- часто причиной окисления металла являются блуждающие токи, присутствующие на поверхности изделия;
- атмосфера с различным содержанием химически активных элементов также может вызвать увеличение скорости распространения коррозии.
На начальном этапе окисления на поверхности металла становятся заметны яркие пятна, впоследствии металл полностью покрывается ржавчиной. Если не обращать внимания на подобные явления, со временем коррозия проникает внутрь изделия, полностью разрушая его.
Разновидности коррозийных процессов
Коррозия стали по типу может быть химической и электротехнической. В первом случае атомы металла и окислителя вступают в реакцию и образуют прочные связи. Образовавшаяся структура не проводит электричество, в отличие от первоначального состава изделия. Для электротехнической коррозии характерно полное разложение металла, который становится непригоден в дальнейшей эксплуатации.
Кроме химической и электротехнической можно выделить и другие виды коррозии:
- чаще других встречается газовая коррозия, протекающая при высокой температуре и минимальном содержании влаги в рабочей среде;
- атмосферная коррозия развивается при нахождении металлического изделия в газовой среде высокой влажности;
- биологические микроорганизмы также могут оказывать негативное влияние на прочность и целостность стальных конструкций, вызывая окисление материала;
- при взаимодействии различных металлов, состав и стационарный потенциал которых отличается, пятна ржавчины могут появиться в точках соприкосновения изделий;
- воздействие радиоактивного излучения приводит к разрушению структуры стали и развитию коррозийных процессов.

В большинстве случаев сложно выделить какой-то один вид коррозии, негативно воздействующий на состояние металлоконструкций. Разрушение и деградация стали вызвана влиянием нескольких факторов, таких как повышенная влажность, неблагоприятный состав атмосферы, биологическая активность микроорганизмов, радиационный фон. Единственным способом исключить или снизить скорость распространения коррозии является защита материала специальными составами и средствами.
Технология защиты стали от возникновения и развития коррозии
Оптимальным вариантом для исключения коррозии является использование при строительстве и монтаже специальных марок стали, неподверженных окислению. В противном случае от собственника металлоконструкций потребуется обеспечить своевременную защиту стали от окисления. Возможными вариантами подобного подхода являются:
- поверхностная обработка металла специальными составами, устойчивыми к атмосферным воздействиям;
- металлизация конструкций, также выполняемая поверхностным методом;
- легирование стали специальными составами, особенностью которых является устойчивость к окислительным процессам;
- непосредственное воздействие на окружающую химическую среду с целью изменения ее состава.

Каждая из указанных методик имеет свои достоинства и условия использования. Выбор способа зависит от текущего состояния стальной конструкции, интенсивности развития коррозии, условий эксплуатации металлических изделий.
Поверхностная обработка металла
Самым простым и наиболее распространенным способом является механическая обработка стали. Конструкция окрашивается эмалями и красками с высоким содержанием алюминия. В результате полностью перекрывается доступ окружающего воздуха к металлу. Простота и невысокая стоимость технологии являются ее основными достоинствами. К минусам можно отнести недолговечность покрытия и необходимость периодически его обновлять.
Химическая обработка металла
Отличным способом защиты стали от коррозии является ее обработка химическим способом. На поверхности создается тонкая и прочная пленка, наличие которой предотвращает проникновение к металлу влаги и других негативных сред. Технология применяется только с использованием специальных средств, а ее стоимость доступна не каждому собственнику металлоконструкций.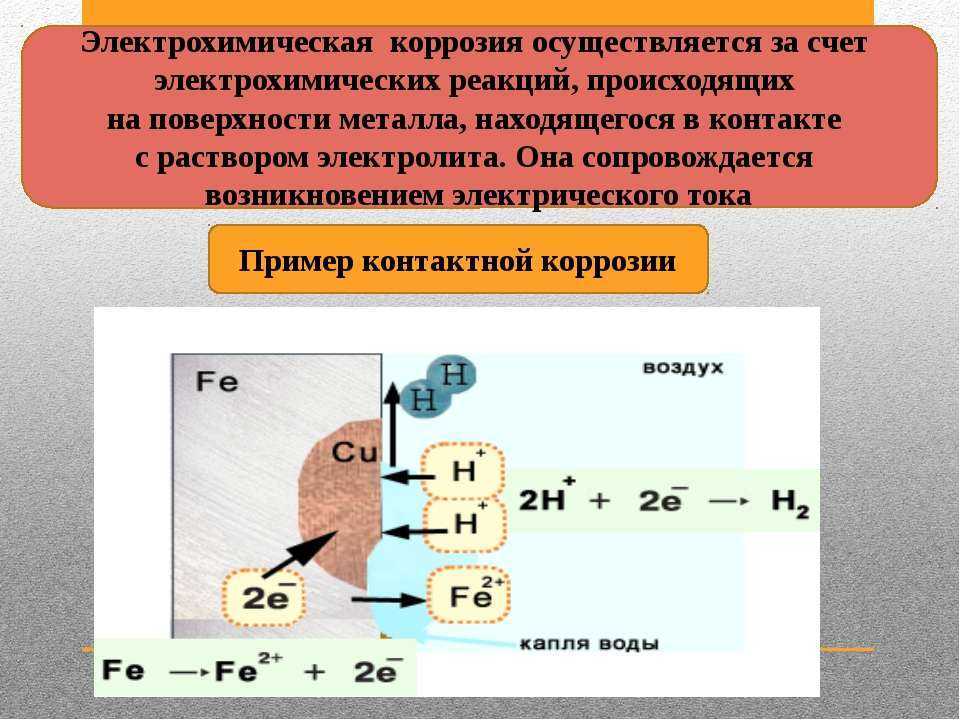
Металлизация и легирование
Нанесение слоя цинка, хрома, серебра или алюминия также является отличным способом обработки стали. Металлизация и легирование позволяет создать на поверхности стали дополнительный слой металла, устойчивого к воздействию окружающей среды. Способ обработки меняется в зависимости от используемого сплава, эффективность метода доказана на практике.
Изменение окружающей среды
Для многих металлоконструкций и изделий, работающих в замкнутом пространстве, гораздо выгоднее создать благоприятные условия. В таких случаях используется технология вакуумирования, в камеру закачивают различные по составу газы. В результате исключается контакт металла и окружающей среды, процессы коррозии полностью отсутствуют.
Каждая из указанных технологий имеет свой диапазон использования. При этом бороться с коррозией необходимо сразу после начала использования металлоконструкций. В противном случае окисление металла будет необратимым, изделие придется ремонтировать или полностью менять гораздо раньше требуемого срока эксплуатации.
Коррозия металлов и защита от коррозии
Коррозия металлов
Коррозия — это разрушение металла под действием окружающей среды.
По механизму протекания различают два типа коррозии — химическую и электрохимическую.
Химическая коррозия начинает влиять на металл сначала его происхождения. Окалина ее продукт. Взаимодействие металла и окружающей среды протекает постоянно, химические процессы, проходящие при этом взаимодействии можно назвать борьбой за выживание, наша задача свести потери металла в этой борьбе к минимуму.
По характеру агрессивной среды различают атмосферную коррозию, подземную и подводную.
Виды коррозионных разрушений разнообразны — равномерная коррозия, неравномерная, коррозия пятнами, коррозия язвами, подповерхностная коррозия, точечная или питтинговая, структурно-избирательная коррозия, межкристаллитная коррозия (этот самый опасный вид коррозии, обусловленный сложностью выявления). Последствия скрытно протекающих коррозионных процессов зачастую приводят к авариям, которых могло бы и не быть.
Последствия скрытно протекающих коррозионных процессов зачастую приводят к авариям, которых могло бы и не быть.
Химическая коррозия — это процесс разрушения металла под действием внешней среды, не сопровождаемая образованием электрического тока. Ее разновидность — газовая коррозия, представляет собой процесс взаимодействия газов при высокой температуре с металлом. При таком взаимодействии образуется оксидная пленка, на железе она рыхлая, легко отскакивает и не защищает от разрушения. В отличии от химической — электрохимическая коррозия протекает при контакте металла с раствором электролита. При этом электролитом может являться любая жидкость или газ. Примером электрохимической коррозии может быть атмосферная коррозия.
Электрохимическая коррозия, более трудно прогнозируемая, чем химическая, ввиду необходимости учёта множества факторов, зачастую изменяющихся в процессе эксплуатации ТУ. При этом скорость протекания процессов электрохимической коррозии на порядок больше чем при химической коррозии. В одних случаях на поверхности металла может образоваться плотная оксидная пленка, выполняющая роль защитного слоя. Образовавшаяся оксидная пленка предохраняет металл от разрушения. Это явление широко используется в современной технике, как способ защиты от коррозионных процессов.
В одних случаях на поверхности металла может образоваться плотная оксидная пленка, выполняющая роль защитного слоя. Образовавшаяся оксидная пленка предохраняет металл от разрушения. Это явление широко используется в современной технике, как способ защиты от коррозионных процессов.
Защита от коррозии
Существует немало способов защиты от коррозии. Самый лучший из них создание такого металла, который бы вообще не коррозировал. Один из путей создания коррозионностойкого металла — получение особых сплавов, в которые добавляют хром, никель, молибден, титан и другие компоненты. Так называемое легирование. Технология создания таких сплавов трудоемка, и связана с повышенными экономическими затратами. Цена таких материалов выше и не всегда целесообразно применение их в конкретных условиях.
Ингибирование — способ, при котором скорость коррозии снижается, если в агрессивную среду ввести соединения, значительно замедляющие коррозионный процесс. Одним из механизмов ингибирования является адсорбция ингибитора на поверхности защищаемого изделия. Ингибируемые бумаги и пленки применяются при долговременном хранении.
Одним из механизмов ингибирования является адсорбция ингибитора на поверхности защищаемого изделия. Ингибируемые бумаги и пленки применяются при долговременном хранении.
Различают металлические и неметаллические защитные покрытия, изолирующие металл от агрессивной среды. Большие детали или трубы защищают методом металлизации.
Плакирование — метод защиты металла от коррозии другим металлом, который устойчив к агрессивной среде. Трубы газо- и нефтепроводов защищаются комбинированным способом, мазутно-битумное покрытие, ингибированная бумага и одновременно с этим катодная защита.
Сущность электрозащиты состоит в том что, на катод, которым является сам трубопровод, накачиваются электроны от внешнего источника тока, и это тормозит коррозию. Анодом в этом случае может служить любой ненужный металл.
Так же широко сейчас применяются различные плёнки на основе полиэтилена, внутренняя поверхность так же защищается различными покрытиями на основе керамики.
Сварные стыки также защищаются от взаимодействия с перекачиваемой средой различными способами. При защите ТУ применяется метод протекторной защиты. Протектор — активный металл, с более отрицательным потенциалом, например цинк, который разрушаясь сам, защищает объект.
Надежным способом зашиты от коррозии, являются гальванические покрытия, которые получают электролизом в водных растворах.
Неметаллические покрытия — это покрытия лаками, красками, различными силикатными эмалями и полимерными материалами. Покрытие силикатными эмалями широко применяется в химической промышленности. Кислотостойкие эмали применяют для покрытия вакуумных аппаратов, резервуаров, реакторов. Затраты на защиту металла от коррозии оправданы и дают хороший экономический эффект, с учётом снижения затрат на замену непригодного ТУ. Где то, например подземные трубопроводы с агрессивной средой, она просто необходима для безопасной эксплуатации.
При проведении экспертизы промышленной безопасности технических устройств, применяемых на опасных производственных объектах, одной из важнейших задач является определение скорости коррозии и прогнозирование этой скорости на планируемый период эксплуатации. Мероприятия по антикоррозионной защите могут значительно увеличить срок эксплуатации и, как следствие, снизить затраты на замену ТУ.
Коррозия металлов. Виды и особенности. Защита и принцип действия
Коррозия металлов – это процесс разрушения металлической поверхности в результате неблагоприятного воздействия окружающей среды. Ее причиной является термодинамическая неустойчивость материала к влиянию различных веществ, которые с ним контактируют.
Разрушение поверхностей наступает вследствие химического или электрохимического взаимодействия неблагоприятной среды. Обе разновидности являются одинаково пагубными для изделий из металла.
Химическая коррозия
Данный процесс осуществляется в среде, которая не производит передачу электрического тока. Он наблюдается, например, при нагреве, в результате чего осуществляется образование химических соединений, таких как сульфиды, а также различные виды пленок. Нередко образованные сплошные пленки становятся непроницаемыми и консервируют поверхность, поэтому последующая коррозия металлов останавливается. Такой защитный слой можно встретить на поверхности из алюминия, хрома, никеля и свинца. Пленка на стали или чугуне является непрочной, поэтому ее наличие не останавливает дальнейшее продвижение разрушения вглубь материала.
Он наблюдается, например, при нагреве, в результате чего осуществляется образование химических соединений, таких как сульфиды, а также различные виды пленок. Нередко образованные сплошные пленки становятся непроницаемыми и консервируют поверхность, поэтому последующая коррозия металлов останавливается. Такой защитный слой можно встретить на поверхности из алюминия, хрома, никеля и свинца. Пленка на стали или чугуне является непрочной, поэтому ее наличие не останавливает дальнейшее продвижение разрушения вглубь материала.
Химическая коррозия может быть двух видов:
- Газовой.
- Жидкостной.
Газовая возникает в результате действия агрессивной газовой среды или пара на поверхность металла, что сопровождается повышенными температурами. Благодаря горячей среде на поверхности отсутствует конденсат. В качестве газа может применяться кислород, диоксид серы, водяной пар, сероводород и так далее. Подобное коррозийное влияние может вызывать абсолютное разрушение активного металла, за исключением случаев, когда образуется защитная непроницаемая пленка.
Жидкостная коррозия металлов возникает в жидкостных средах, которые не способны передавать электричество. В первую очередь она наблюдается при контакте металлов с сырой нефтью, нефтепродуктами или смазочными маслами. При наличии в таких веществах небольшой доли воды, коррозия переходит в электрохимическую.
В обоих вариантах химической коррозии скорость разрушения является пропорциональной химической реакции, с которой окислитель проникает сквозь созданную оксидную пленку на поверхности.
Электрохимическая коррозия металлов
Эта разновидность разрушения поверхности металла происходит в среде, которая может передавать электрический ток. В результате данного процесса наблюдается изменение состава металла. Атомы удаляются от кристаллической решетки в результате анодного или катодного воздействия. При анодном влиянии ионы металла переходят в раствор жидкости, которая его окружает. При катодном влиянии получаемые при анодном процессе электроны связываются с окислителем. Наиболее распространенной является электрохимическая коррозия под воздействием водорода или кислорода.
Наиболее распространенной является электрохимическая коррозия под воздействием водорода или кислорода.
Процесс влияния электрохимической коррозии на металлы зависит от уровня их активности. По данному критерию их разделяют на 4 группы:
- Активные.
- Средней активности.
- Малоактивные.
- Благородные.
Активные имеют высокую нестабильность. Для них характерно возникновение коррозии даже в нейтральной водной среде, которая лишена растворенного кислорода или окислителей. Ярким представителем такого металла является кадмий.
Металлы средней активности располагаются на таблице химических элементов между кадмием и водородом. Они неподвержены началу разрушения в нейтральной жидкостной среде лишенной кислорода, но начинают интенсивно поддаваться коррозии при влиянии кислот.
Малоактивные металлы располагаются в таблице Менделеева между водородом и родием. Они не подвергаются влиянию коррозии при контакте с нейтральными жидкостями и кислой средой. Для активизации процесса их разрушения необходимо наличие кислорода или прочих окислителей.
Для активизации процесса их разрушения необходимо наличие кислорода или прочих окислителей.
Благородные металлы отличаются стабильностью, благодаря чему подвержены коррозии только при воздействии кислой среды при условии контакта с сильными окислителями. К перечню благородных металлов относится платина, золото, палладий и иридий.
Электрохимическая коррозия металлов является самой распространенной, поскольку естественные условия, в которых хранятся и эксплуатируются металлические изделия, зачастую подвержены влиянию влажной среды.
Различают следующие виды электрохимической коррозии:
- Электролитная – наблюдается при контакте с растворами солей, кислотами, оснований, в том числе и обычной водой.
- Атмосферная – наблюдается в условиях атмосферы, где содержатся испарения воды. Данный вид является самым распространенным, именно он влияет на практически все металлические изделия.
- Почвенная – наблюдается в результате воздействия влажной почвы, в составе которой могут содержаться различные химические элементы ускоряющие процесс разрушения металла.
 При воздействии с кислыми почвами процесс коррозии наблюдается наиболее агрессивно. Грунты с песком воздействуют медленней всего.
При воздействии с кислыми почвами процесс коррозии наблюдается наиболее агрессивно. Грунты с песком воздействуют медленней всего. - Аэрационная – является более редкой и наблюдается в тех случаях, если к разным поверхностям металла оказывается неравномерный доступ воздуха. В результате неоднородного воздействия линии переходов между такими участками начинают разрушаться.
- Морская коррозия металлов подразумевает разрушение от влияния морской воды. Она выделяется в отдельную группу, поскольку данная жидкость отличается высоким содержанием солей и растворенных органических веществ. Это делает ее более агрессивной.
- Биокоррозия – данный вид разрушения возникает при условии воздействия на поверхность металла бактериями, которые в результате жизнедеятельности вырабатывают углекислый газ и прочие вещества.
- Электрокоррозия – такой вид разрушения металла наблюдается при воздействии на него блуждающих токов, что характерно для подземных сооружений, в частности рельсов метрополитена, стержней заземления, трамвайных линий и т.
 д.
д.
Методы защиты от коррозии
Голая поверхность подавляющего большинства металлов склонна к быстрой коррозии, поэтому для снижения разрушающего воздействия применяются различные способы защиты.
Покрытие изоляционными слоями:
- Другим металлом.
- Цементным раствором.
- Лаками.
- Красками.
- Битумом.
Одним из самых эффективных способов защиты от коррозии является покрытие поверхности одного металла другим, менее склонным к коррозии. Примером такого технического решения является оцинковка, когда сталь защищается слоем цинка. Внутренний металл полностью изолирован до тех пор, пока цинк в результате естественной коррозии, которая протекает очень медленно, полностью не разрушится, оголив сталь. Такой метод защиты является одним из самых эффективных, поскольку покрывной металл полотна удерживается на основании, поэтому его невозможно срывать слоями. Недостаток метода заключается в том, что при механическом воздействии можно сцарапывать тонкую защитную пленку.
Покрытие металла защитным цементным раствором, битумом, лаками и красками является также очень распространенным решением, которое все же уступает оцинковке. Это связано с неоднородностью составов основания и покрытия. В результате низкой адгезии краски готовое покрытие будет отслаиваться. Такая защита может покрываться трещинами, обеспечивая доступ влаги.
Коррозия металлов может быть приостановлена при наличии химического покрытия:
- Оксидирование.
- Фосфатирование.
- Азотирование.
- Воронение.
- Цементация.
Поверхность металла подвергается влиянию различных веществ, фосфатов, азота или оксидов, в результате чего создаются пленки, которые благодаря своей непроницаемости предотвращают разрушение. Такие методы применимы в первую очередь для сталей. Также распространенным решением является воронение стали, когда поверхность металла взаимодействует с органическими веществами. Обработанные таким способом поверхности приобретают темный цвет, напоминающий крыло ворона, за что данный метод и получил свое название. Одним из наиболее эффективных вариантов химического покрытия является цементация, когда на поверхность воздействуют углеродом, в результате чего создается корка вступившего в реакцию металла.
Одним из наиболее эффективных вариантов химического покрытия является цементация, когда на поверхность воздействуют углеродом, в результате чего создается корка вступившего в реакцию металла.
Для защиты от коррозии черных металлов может применяться технология изменения их состава. Добавление различных соединений позволяет получить сплавы, отличающиеся большей устойчивостью к коррозии. Примером такого соединения является нержавеющая сталь.
Самым необычным является протекторная защита, которая подразумевает покрытие сооружений из одного металла пластинами из более активного металла, так называемого протектора. Поскольку он имеет более отрицательный потенциал, то выступает в роли анода. Защищаемая поверхность используется как катод. Они соединяются между собой проводником тока, благодаря чему создаются неблагоприятные условия для протектора. Как следствие разрушению поддается именно он, в то время как ценное сооружение остается целым.
Более редким решение является изменение состав окружающей среды.
 В таких условиях коррозия металлов замедляется или не происходит. Данный метод подразумевает очистку состава жидкости или газа от кислот и солей, вызывающих разрушение. Такой метод применим далеко не во всех случаях, поскольку отличается техническими сложностями и определенной дороговизной. Его используют в разных механизмах. К примеру, могут применять в определенных средах только те металлы, для которых те не агрессивны.
В таких условиях коррозия металлов замедляется или не происходит. Данный метод подразумевает очистку состава жидкости или газа от кислот и солей, вызывающих разрушение. Такой метод применим далеко не во всех случаях, поскольку отличается техническими сложностями и определенной дороговизной. Его используют в разных механизмах. К примеру, могут применять в определенных средах только те металлы, для которых те не агрессивны.
Похожие темы:
- Степень защиты IP. Маркировка. Выбор устройств
- Преобразователь ржавчины. Виды и работа. Применение
Методы и способы защиты от коррозии металлов
Проблема изыскания новых и совершенствование старых способов защиты от коррозии актуальна, как для всей тяжёлой промышленности в целом, так и для автомобильной отрасли в частности.
Еще в XIX веке лучшие инженерные умы того времени волновала проблема защиты металлических конструкций от ржавления. Например, Александр Гюста́в Э́йфель, отец и создатель знаменитой «Tour de 300 mètres», говорил: «Трудно переоценить роль краски в сохранении металлического сооружения, и забота об этом – единственная гарантия его долголетия».
Портрет Александра Гюста́ва Э́йфель и его творение — Эйфелева башня
Кстати, вот уже 131 год эта достопримечательность Парижа противостоит воздействию неблагоприятных факторов окружающей среды именно благодаря краске. Интересный факт – для защиты 200.000 м2 наружной поверхности башни используется около 60 тонн специальной краски. Покраской занимается обслуживающая Эйфелеву башню специально созданная компания «SETE» («Société Nouvelle d’exploitation de la Tour Eiffel»). Весь процесс окраски занимает около 18 месяцев! Вначале, все детали конструкции тщательно осматриваются. Те, на которых слой антикоррозионного покрытия нарушен, – очищаются от старого и покрываются новым. Кроме того, вся поверхность сооружения перед окраской очищается паром высокого давления. Красят башню в два слоя.
Но, окрашивание защищаемой поверхности – всего лишь один из способов защиты металла от коррозии. Применительно к автомобилестроению, все методы защиты можно условно разделить на следующие виды:
1. Нанесение защитных покрытий (металлических и неметаллических).
Нанесение защитных покрытий (металлических и неметаллических).
2. Изменение характеристик коррозионной среды.
3. Легирование.
4. Электрохимическая защита
5. Рациональное конструирование.
Нанесение защитных покрытий
Нанесение защитных покрытий – один из самых простых, а также исторических старых способов защиты металла от коррозии. Различают металлические и неметаллические покрытия. В свою очередь неметаллические покрытия делят на органические и неорганические.
Органические покрытия – это, привычные нам, лак и краска, а также разнообразные смолы. Сюда же относят полимерные плёнки и резину.
Неорганические покрытия включают в себя разнообразные эмали и грунты на основе соединений кремния, фосфора, цинка и хрома, а также оксидов металлов (например, оксид титана). Классическим примером использования неорганического покрытия в автомобилестроении является процесс фосфатирования автомобильных кузовов. Так, слоем фосфатов перед покраской покрывают кузова автомобилей на заводах Mercedes-Benz.
Так, слоем фосфатов перед покраской покрывают кузова автомобилей на заводах Mercedes-Benz.
Металлические покрытия (анодные и катодные) представляют собой нанесённый на защищаемую поверхность слой металла (цинк, хром, кадмий, алюминий и др.) или металлического сплава (олово, бронза, латунь и т.д.). У анодного покрытия электродный потенциал меньше электродного потенциала защищаемого металла. Поэтому, при повреждении анодного покрытия в первую очередь будет окисляться непосредственно оно само. В случае с катодным металлическим покрытием – наоборот: электродный потенциал покрытия выше потенциала защищаемого металла. Значит, при повреждении такого покрытия первой будет окисляться сама защищаемая поверхность.
Нанесение антикоррозийной защиты Krown
Цинкование
Применительно к автомобилестроению, классическим примером защиты с помощью металлического покрытия является оцинкованный автомобильный кузов. Этот способ получил очень широкое распространение и на сегодняшний день целый ряд автопроизводителей используют цинкование для защиты кузовных деталей. Но, первопроходцем в этом деле стала немецкая компания Audi, впервые применившая оцинковку для защиты кузовов своих автомобилей. Не остановившись на этом, инженеры Audi AG разработали и внедрили в производство двухстороннюю цинковую защиту не только кузовных деталей, но и их сварных соединений, а также и самих кузовов в целом. (Метод т.н. «горячего» цинкования погружением в ванну.) Первым серийным автомобилем с полностью оцинкованным кузовом стал Audi 80 B3, впервые сошедший с конвейера в уже далеком 1986 году.
Этот способ получил очень широкое распространение и на сегодняшний день целый ряд автопроизводителей используют цинкование для защиты кузовных деталей. Но, первопроходцем в этом деле стала немецкая компания Audi, впервые применившая оцинковку для защиты кузовов своих автомобилей. Не остановившись на этом, инженеры Audi AG разработали и внедрили в производство двухстороннюю цинковую защиту не только кузовных деталей, но и их сварных соединений, а также и самих кузовов в целом. (Метод т.н. «горячего» цинкования погружением в ванну.) Первым серийным автомобилем с полностью оцинкованным кузовом стал Audi 80 B3, впервые сошедший с конвейера в уже далеком 1986 году.
Процесс цинкования
Изменение характеристик коррозионной среды
Изменение характеристик коррозионной среды – суть этого метода защиты заключается в том, что для снижения агрессивности среды в ней уменьшают количество опасных в коррозионном отношении компонентов или же применяют ингибиторы коррозии. (Это специальные вещества, замедляющие её скорость.) И вот, казалось бы, неразрешимая дилемма – как можно снизить количество опасных для стальных деталей автомобиля химических соединений в городской среде? Да очень просто – для начала перестать сыпать на дороги зимой активаторы коррозии, к примеру, тот же хлорид натрия. (О его роли в химическом процессе ржавления автомобиля мы говорили в первой части нашего рассказа.)
(Это специальные вещества, замедляющие её скорость.) И вот, казалось бы, неразрешимая дилемма – как можно снизить количество опасных для стальных деталей автомобиля химических соединений в городской среде? Да очень просто – для начала перестать сыпать на дороги зимой активаторы коррозии, к примеру, тот же хлорид натрия. (О его роли в химическом процессе ржавления автомобиля мы говорили в первой части нашего рассказа.)
Что касается ингибиторов коррозии, то их целесообразно использовать в замкнутых системах (где редко или мало обновляется циркулирующая жидкость). В автомобилестроении типичным примером таковой является система охлаждения двигателя. А все современные антифризы в обязательном порядке содержат в себе ингибиторы коррозии.
Легирование
Легирование (от немецкого legieren – «сплавлять» и от латинского ligare – «связывать») – один из самых эффективных и, одновременно, дорогих способов борьбы со ржавчиной. Суть этого метода заключается в том, что в состав стали добавляют т. н. «легирующие элементы». Таковыми являются некоторые металлы: хром, никель, марганец, ванадий, ниобий, вольфрам, молибден, титан, медь. Данные компоненты придают сплаву пассивность – т.е. при начале коррозии образуются плотные поверхностные продукты реакции, предохраняющие металл от дальнейшего коррозионного разрушения.
н. «легирующие элементы». Таковыми являются некоторые металлы: хром, никель, марганец, ванадий, ниобий, вольфрам, молибден, титан, медь. Данные компоненты придают сплаву пассивность – т.е. при начале коррозии образуются плотные поверхностные продукты реакции, предохраняющие металл от дальнейшего коррозионного разрушения.
Легированные стали, устойчивые к коррозии в атмосфере и агрессивных средах, также называют «нержавеющими сталями», или же, в простонародье, «нержавейкой». Если говорить об её применении в машиностроении, то нужно сказать, что изготовить кузов автомобиля целиком из нержавеющего сплава, конечно же, возможно. Вот только никакой целесообразности в этом нет, ибо цена такой машины будет астрономической. Причина – изначально высокая стоимость коррозионно-стойкой стали. Тем не менее, в автомобилестроении она активно используется. Так, из неё изготавливают детали системы выпуска отработанных газов и термоотражающие экраны.
Электрохимическая защита
Электрохимическая защита автомобиля
Если говорить о методе электрохимической защиты, то, применительно к автомобилестроению, он является малоиспользуемым. Его суть заключается в торможении протекающих при электрохимической коррозии процессов (катодного / анодного). Например, к защищаемому элементу присоединяется деталь из более активного, нежели сам элемент, металла. В образовавшейся гальванической (коррозионной) паре в первую очередь будет разрушаться активный металл (протектор).
Его суть заключается в торможении протекающих при электрохимической коррозии процессов (катодного / анодного). Например, к защищаемому элементу присоединяется деталь из более активного, нежели сам элемент, металла. В образовавшейся гальванической (коррозионной) паре в первую очередь будет разрушаться активный металл (протектор).
А вот метод рационального конструирования, в силу своей относительной простоты и малозатратности, наоборот, получил широкое распространение в машиностроении. Суть его заключается в том, что при проектировании узлов и агрегатов по возможности пытаются уменьшить площадь контакта с агрессивной средой опасных в коррозионном отношении участков деталей (сварных швов и металлических соединений). Если, в силу особенностей конструкции, сделать это не представляется возможным, предусматривают защиту данных узлов от коррозии различными вышеуказанными методами.
Для скачивания — Кафедра химии
- Главная
- Университет
- Для скачивания
- Кафедра химии
Лекция. Растворы неэлектролитов
Растворы неэлектролитов
Размер файла:
638.79 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Растворы неэлектролитов. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ , 2016. – 33 с.
Учебно-методическое пособие включает лекцию по теме «Растворы неэлектролитов» курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование пособия, в котором рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Окислительно-восстановительные реакции
Размер файла:
609.98 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Окислительно – восстановительные реакции. Лекция по курсу «Общая химия » для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 31 с.
– 31 с.
Учебно-методическое пособие включает лекцию по теме «Окислительно – восстановительные реакции» и предназначено для контролируемой самостоятельной работы студентов инженерно–технологического факультета. Использование такого пособия, в котором рассмотрены важнейшие вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Комплексные соединения
Размер файла:
531.46 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Лекция «Комплексные соединения» по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 26 с.
Учебно-методическое пособие включает лекцию по теме «Комплексные соединения» курса «Общая химия». Комплексные соединения играют важную роль в природе и технике, прежде всего, это ферментативные и фотохимические процессы, перенос кислорода в биологических системах, тонкая технология редких металлов, каталитические реакции и т. д. Координационные свойства проявляются всеми элементами периодической системы.
д. Координационные свойства проявляются всеми элементами периодической системы.
Скачать
Лекция. Кинетика химических реакций. Химическое равновесие
Размер файла:
768.32 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Кинетика химических реакций. Химическое равновесие. Лекции по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 44 с.
Учебно-методическое пособие включает лекции по отдельным темам курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование таких пособий, в которых рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Предэкзаменационные тесты по органической и биологической ХИМИИ
Размер файла:
1.30 MB
Автор:
Макарчиков А.Ф., Колос И.К.
Дата:
26. 12.2016 12:02
12.2016 12:02
Предэкзаменационные тесты по органической и биоло-гической химии для студентов биотехнологического факультета / А.Ф. Макарчиков, И.К. Колос – Гродно: ГГАУ, 2016. – 205 с.
В пособии приведен перечень вопросов для проведения предэкзаменационного тестирования студентов, обучающихся на биотехнологическом факультете, по предмету «Химия (органическая и биологическая)»
Скачать
Лекция. Электролиз. Коррозия металлов и методы защиты металлов от коррозии
Размер файла:
758.87 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:02
Электролиз. Коррозия металлов и методы защиты металлов от коррозии. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 31 с.
Учебно-методическое пособие включает лекции по отдельным темам курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование таких пособий, в которых рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Энергетика химических процессов.
Размер файла:
604.00 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:02
Энергетика химических процессов. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 25 с.
Учебно-методическое пособие включает лекцию по теме «Энергетика химических процессов» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование такого пособия, в котором рассмотрены важнейшие вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Строение атомов элементов
Размер файла:
789.90 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:02
Строение атомов элементов. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ , 2016. – 23 с.
– 23 с.
Учебно-методическое пособие включает лекцию по теме «Строение атомов элементов» курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование пособия, в котором рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Основные понятия и законы химии
Размер файла:
675.23 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Основные понятия и законы химии. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 30 с.
Учебно-методическое пособие включает лекцию по теме «Основные понятия и законы химии» курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование студентами распечатки лекционной темы значительно сэкономит время для понимания материала, излагаемого лектором, и конспектирования.
Скачать
Предэкзаменационные тесты по химии
Размер файла:
813.02 kB
Автор:
Макарчиков А.Ф., Колос И.К.
Дата:
14.11.2016 11:47
Предэкзаменационные тесты по химии для студентов, обучающихся на агробиологических специальностях / А.Ф. Макарчиков, И.К. Колос – Гродно: ГГАУ, 2016. – 201 с.
В пособии приведен перечень вопросов для проведения предэкзаменационного тестирования студентов, обучающихся на агробиологических специальностях, по предмету «Химия».
Скачать
Методическое пособие для лабораторных работ по аналитической химии
Размер файла:
544.41 kB
Автор:
Апанович З.В., Тараненко Т.В., Томашева Е.В., Кулеш И.В., Цветницкая Э.В.
Дата:
28.12.2015 12:22
В пособие излагается материал по аналитической химии в объеме соответствующих программ по специальностям: «Ветеринарная медицина», «Аграномия», «Биотехналогия». Содержатся методические указания по технике выполнения лабораторных работ по качественному и количественному анализу.
Скачать
Комментарии для работы с рабочими тетрадями по химии элементов
Размер файла:
655.75 kB
Дата:
28.12.2015 12:22
Комментарии для работы с рабочими тетрадями по химии элементов / З.В. Апанович, Ю.А. Лукашенко.
Учебно-методическое пособие включает лекции по отдельным темам курса «Неорганическая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета, для которых введен отдельный курс по химии элементов, а также может быть использовано студентами других факультетов.
Скачать
Практикум по физической химии
Размер файла:
1.03 MB
Дата:
01.04.2013 04:24
Учебно-методическое пособие (для проведения лабораторных занятий) для студентов инженерно-технического факультета
Практикум по физической химии: учеб.-мет. пособие / О. И. Валентюкевич.- Гродно: ГГАУ, 2008 – 88с.
Данное пособие предназначено для студентов технологических специальностей аграрного университета. Целью данного пособия является оказание помощи в изучении теоретического материала, а также выработка навыков экспериментальной работы.
Целью данного пособия является оказание помощи в изучении теоретического материала, а также выработка навыков экспериментальной работы.
Скачать
Коллоидная химия
Размер файла:
834.37 kB
Дата:
01.04.2013 04:09
Учебно-методическое пособие (для проведения лабораторных занятий) для студентов инженерно-технического факультета
К-60 Практикум по физической химии: учеб.-мет. пособие / И. В. Кулеш, О. И. Валентюкевич.- Гродно: ГГАУ, 2013 – 94с.
Данное пособие предназначено для студентов технологических специальностей аграрного университета. Целью данного пособия является оказание помощи в изучении теоретического материала, а также выработка навыков экспериментальной работы.
Скачать
Курс лекций по дисциплине «Неорганическая химия»
Размер файла:
1.33 MB
Дата:
28.12.2015 12:22
Лекции по курсу «Неорганическая химия »для студентов инженерно – технологического факультета / З.В. Апанович.
Скачать
Рабочая тетрадь и методические указания по неорганической химии
Размер файла:
701. 32 kB
32 kB
Дата:
28.12.2015 12:23
Рабочая тетрадь и методические указания по неорганической химии. Для студентов технологических специальностей / З.В. Апанович.
Скачать
Ионные равновесия и обменные реакции в растворах электролитов
Скачать
Лабораторные работы по химии элементов для студентов технологических специальностей
Скачать
Университет
Как защитить металлы – AMPP
Коррозия – это естественный износ, возникающий в результате химической или электрохимической реакции металла или металлического сплава с окружающей средой. Подобно другим стихийным бедствиям — землетрясениям, торнадо, наводнениям — коррозия может нанести опасный и дорогостоящий ущерб всему, от транспортных средств, бытовой техники и систем водоснабжения/очистки до трубопроводов, мостов и общественных зданий. Коррозия отличается от других стихийных бедствий тем, что существуют проверенные временем методы, а также новые технологии, которые помогают контролировать и предотвращать коррозию, тем самым защищая людей, имущество и планету от ее негативного воздействия.
Перед определением конкретной проблемы и/или решения по предотвращению и контролю коррозии необходимо учитывать множество факторов, включая, помимо прочего:
- условия окружающей среды (удельное сопротивление почвы, влажность и воздействие соленой воды на различные типы материалов )
- тип продукта, подлежащего обработке, обработке или транспортировке
- требуемый срок службы конструкции или компонента
- близость к явлениям, вызывающим коррозию
Несмотря на это, казалось бы, сложное взаимодействие факторов и почти неизбежную ржавчину металлов, коррозия является контролируемым процессом, когда такие широко используемые и эффективные методы выбора и проектирования материалов, защитных покрытий, измерений и контроля, катодной защиты, химических ингибиторов и управления коррозией считаются.
Выбор материалов и проектирование
Тщательное и реалистичное рассмотрение вопросов предотвращения коррозии и смягчения ее последствий на этапе выбора материалов в процессе проектирования имеет решающее значение для предотвращения многих типов отказов.
Факторы, которые могут повлиять на выбор материалов, включают коррозионную стойкость в окружающей среде, наличие проектных данных и данных испытаний, механические свойства, стоимость, доступность, ремонтопригодность, совместимость с другими компонентами системы, ожидаемый срок службы, надежность и внешний вид.
Неотъемлемой частью выбора материалов является соответствующий проект системы, учитывающий параметры процесса и конструкции; геометрия для дренажа; предотвращение или электрическое разделение разнородных металлов; предотвращение или герметизация щелей; допуск на коррозию; срок эксплуатации; требования к техническому обслуживанию и осмотру.
В то время как использование металлов и бетона является обычным выбором при проектировании, наука о материалах предлагает инженерам-коррозионистам варианты борьбы с коррозией с использованием современных материалов. Инженерные свойства, созданные с помощью специализированных технологий обработки и синтеза, придают усовершенствованным материалам превосходные характеристики по сравнению с обычными материалами и включают керамику, металлы с высокой добавленной стоимостью, электронные материалы, композиты, полимеры и биоматериалы.
Ресурсы по выбору материалов и проектированию AMPP
Защитные покрытия
Исследование коррозии, проведенное NACE International, теперь AMPP, показывает, что 50% всех затрат на коррозию можно предотвратить, причем примерно 85% из них относится к защитным покрытиям.
Защитные покрытия, включая краски, представляют собой тонкие слои твердого материала, нанесенные на подложку, при этом покрытие действует как барьер, препятствующий или предотвращающий коррозию, износ или воздействие воды. Каждая жидкая, разжижаемая или мастичная композиция после нанесения на поверхность превращается в твердую защитную, декоративную или функциональную клейкую пленку. Покрытия можно напылять, приваривать, гальванизировать или наносить с помощью ручных инструментов в зависимости от поверхности покрытия, окружающей среды и целей нанесения.
Материалы, обычно используемые в органических покрытиях, представляют собой эпоксидные смолы, полиуретаны или другие полимеры, в то время как материалы, обычно используемые в неорганических металлических покрытиях, включают цинк, алюминий и хром.
После подготовки поверхности покрытия наносятся в 3 этапа: сначала грунтовка, затем полное покрытие, а затем герметик.
Учебный центр защитных покрытий | Ресурсы защитных покрытий AMPP
Измерение и проверка
Инспекции покрытий проверяют промышленное оборудование и объекты, а также коммерческую недвижимость и проекты, чтобы убедиться, что защитные покрытия были нанесены правильно, чтобы минимизировать риск коррозии.
Проверка покрытий помогает укрепить всю отрасль защитных покрытий и позволяет сэкономить миллиарды долларов на коррозионных затратах.
Ресурсы для измерения и проверки AMPP
Катодная защита (CP)
Катодная защита — это технология, используемая для контроля коррозии поверхности металла путем превращения ее в катод электрохимической ячейки. CP может быть достигнут путем подачи тока в структуру от внешнего электрода и поляризации металлической поверхности в электроотрицательном направлении. Это обеспечивает защиту поверхности и продлевает срок службы актива.
Системы CP защищают широкий спектр металлоконструкций, включая наземные и морские трубопроводы, резервуары для хранения, сваи причалов, корпуса кораблей и лодок, морские нефтяные платформы и компоненты металлической арматуры в бетонных конструкциях. Другой метод CP для смягчения коррозии включает нанесение цинкового покрытия на компоненты из оцинкованной стали.
Средства катодной защиты AMPP
Химические ингибиторы
Ингибитор коррозии снижает скорость коррозии металла, подвергающегося воздействию окружающей среды, путем замедления химической (коррозионной) реакции.
Чтобы уменьшить интенсивность коррозии, их обычно добавляют в небольших количествах к кислотам, охлаждающей воде, пару и многим другим средам либо постоянно, либо периодически. При использовании в качестве покрытия ингибиторы коррозии обычно наносят на чистые поверхности и дают им проникнуть и высохнуть.
Ингибирование может использоваться внутри труб и сосудов из углеродистой стали в качестве экономичной альтернативы защите от коррозии для нержавеющих сталей и сплавов, покрытий или неметаллических композитов, и часто может применяться без нарушения процесса. Ингибиторы также можно использовать для защиты от коррозии армированных стальных стержней (арматурных стержней) внутри бетона.
Ингибиторы также можно использовать для защиты от коррозии армированных стальных стержней (арматурных стержней) внутри бетона.
Ресурсы химических ингибиторов AMPP
Борьба с коррозией
Для предотвращения коррозии и снижения связанных с ней затрат необходимы не только технологии; для этого требуется упреждающий план управления коррозией для улучшения проектирования, эксплуатации и технического обслуживания критически важных активов. Кроме того, эти планы должны быть основаны на изменении того, как решения по коррозии принимаются внутри организации.
Согласно исследованию NACE, те компании, которые лучше всего справляются с сокращением негативных последствий коррозии, следуют определенным практикам с техническими планами управления коррозией, интегрированными в общую систему управления их организации, таким образом охватывая все уровни организации. Вовлекая каждого сотрудника в план управления коррозией организации, стратегии могут быть реализованы на каждом этапе жизненного цикла продукта или объекта, что приводит к значительной экономии затрат в течение всего срока службы актива.
Ресурсы AMPP по борьбе с коррозией
Понимание коррозии и способы защиты от нее
Ежегодно коррозия машин, зданий и оборудования обходится американской промышленности примерно в 7 миллиардов долларов. Коррозия является дорогостоящей проблемой. Но, поняв его первопричины, можно предпринять эффективные шаги для его предотвращения и борьбы с ним.
Существует несколько видов затрат на коррозию, которые должны учитывать заводчане:
• Прямая потеря или повреждение металлических конструкций из-за коррозии. Примером может служить резервуар для горячей воды, который подвергся коррозии и должен быть утилизирован.
• Затраты на техническое обслуживание, связанные с коррозией. В эту область попадает любая металлическая поверхность, которую необходимо красить каждые несколько лет для борьбы с коррозией.
• Косвенные потери в результате коррозии. Эти потери могут быть результатом утечек и пожаров. Взрывы, связанные с утечкой, перебоями в подаче электроэнергии, остановкой оборудования и потерями рабочей силы, также косвенно являются результатом коррозии.
Первый шаг к управлению этими затратами требует понимания того, что такое коррозия и что ее вызывает.
Что такое ржавчина?
При коррозии железа или стали образуется оксид железа, или то, что мы называем ржавчиной. Сталь в основном состоит из железной руды. В своем естественном состоянии железная руда очень похожа на ржавчину: темно-красная и мелкозернистая, с тенденцией удерживать влагу.
Железная руда является стабильным веществом до тех пор, пока она не будет преобразована в железо или сталь, естественно более слабые элементы. Когда сталь подвергается воздействию влаги и кислорода, она сразу же начинает возвращаться к своему естественному состоянию. Несмотря на принятые защитные меры, большая часть стали, произведенной в этом столетии, уже проржавела до состояния оксида, своего естественного состояния.
Для существования коррозии необходимы три элемента: защищенный металл, корродированный металл и проводящая ток среда между ними. Когда два разнородных металла соприкасаются, один из них становится защищенным металлом, а другой корродирующим. Операторы установки могут распознавать условия окружающей среды, способствующие коррозии.
Операторы установки могут распознавать условия окружающей среды, способствующие коррозии.
Например:
• Если на стальной трубе используются оцинкованные фитинги, оцинкованные (цинковые) фитинги подвергаются коррозии, а сталь остается защищенной.
• Сталь или другие металлы под нагрузкой подвергаются коррозии, в то время как ненагруженная сталь защищена от коррозии. Вот почему вы видите ржавчину на стали.
• Свежеобрезанная сталь быстрее подвергается коррозии. Резьба, нарезанная на трубе, всегда ржавеет первой.
Даже если кусок стали не соприкасается с другим металлом, ни под нагрузкой, ни в свежем состоянии, он будет ржаветь под воздействием погодных условий. Это связано с тем, что сталь не совсем однородна по составу — в одном куске стали могут возникать небольшие вариации плотности и состава, что приводит к коррозии.
Третьим компонентом, необходимым для коррозии стали, является электролит. Обычно это жидкость или водосодержащее вещество, которое проводит ток коррозии от защищаемого металла к корродированному металлу. Наиболее распространенным токопроводящим веществом является вода. Дождь, роса, влажность воздуха и т. д. — все это служит эффективными электрическими проводниками. Сталь очень медленно подвергается коррозии в пустынном климате, где влажность низкая, а осадки редки. В районах с высокой влажностью и частыми дождями защита стали имеет решающее значение. Операторы установок узнают некоторые из следующих сред, в которых электрический ток ускоряет процесс коррозии:
Наиболее распространенным токопроводящим веществом является вода. Дождь, роса, влажность воздуха и т. д. — все это служит эффективными электрическими проводниками. Сталь очень медленно подвергается коррозии в пустынном климате, где влажность низкая, а осадки редки. В районах с высокой влажностью и частыми дождями защита стали имеет решающее значение. Операторы установок узнают некоторые из следующих сред, в которых электрический ток ускоряет процесс коррозии:
• Добавление соли в воду значительно увеличивает ее способность проводить ток. Таким образом, сталь, подвергающаяся воздействию морской воды или соляного тумана, будет корродировать быстрее, чем сталь в пресной воде. Атмосферная коррозия больше проявляется в районах вблизи океанов из-за воздействия соленого воздуха. Концентрированные солевые растворы, например, используемые в пищевой промышленности, вызывают сильную коррозию.
• Промышленные дымы и пары содержат кислоты, щелочи и другие химические вещества, которые служат проводниками тока. Следовательно, атмосферная коррозия в промышленных районах более выражена, чем в сельской местности.
Следовательно, атмосферная коррозия в промышленных районах более выражена, чем в сельской местности.
• Почва, глина и земляные материалы также являются хорошими проводниками электричества. Трубопроводы и другая сталь, зарытая в землю, будут подвержены коррозии, если не будут защищены. Точно так же, как почвы значительно различаются по составу, они также различаются по своей электропроводности: одни почвы вызывают более сильную коррозию, чем другие.
Защита от коррозии
Чтобы сделать использование стали и других металлов практичным в строительстве и производстве, необходимо применять некоторые методы защиты от коррозии. В противном случае срок службы стали и других металлов будет ограничен, что приведет к снижению эффективности и увеличению стоимости обслуживания. Существует несколько эффективных способов остановить коррозию:
1. Впечатанный ток. С помощью подходящего токогенерирующего оборудования и средств управления можно воспроизвести ток, равный по силе корродирующему току, но протекающий в противоположном направлении. Этот тип защиты обычно ограничивается трубопроводами, заглубленными резервуарами и т. д. и требует тщательного проектирования и компоновки. При неправильном использовании подаваемый ток может способствовать коррозии.
Этот тип защиты обычно ограничивается трубопроводами, заглубленными резервуарами и т. д. и требует тщательного проектирования и компоновки. При неправильном использовании подаваемый ток может способствовать коррозии.
2. Жертвенные металлы. Сталь можно защитить, поместив рядом с разнородным металлом. Например, если цинк или магний находятся в непосредственном контакте со сталью, они защищают сталь от коррозии. Здесь цинк и магний служат жертвенными металлами, которые не только защищают область непосредственного контакта, но и защищают за пределами металла в каждом направлении. Защита от ржавчины жертвенными металлами обычно используется в нескольких формах:
• Цинковые или магниевые блоки часто используются для защиты корпусов кораблей, внутренней части резервуаров для воды и других подводных поверхностей.
• Часто производится полное покрытие стали защитным металлом. Оцинкованная сталь, например, это сталь, покрытая цинком. Цинк является жертвенным и защитит базовую сталь.
• Покрытия с высоким содержанием цинка могут быть нанесены на стальную поверхность для обеспечения катодной защиты. Покрытия с высоким содержанием цинка состоят из 85-95% металлического цинка в подходящем связующем. Частицы цинка, нанесенные при окраске, защищают сталь.
3. Грунтовки. Грунтовки и готовые покрытия защищают металлические поверхности, создавая барьер между сталью и корродирующими элементами. Они также предотвращают попадание влаги на поверхность стали. Покрывающая пленка защищает нижележащие металлические подложки тремя способами:
• Покрытия могут замедлять скорость диффузии воды и кислорода из окружающей среды к поверхности металла. Это замедляет процесс коррозии.
• Пленка краски может замедлить скорость диффузии продуктов коррозии с поверхности металла через пленку краски. Это также замедляет процесс коррозии.
• Антикоррозийные пигменты, содержащиеся в качественных грунтовках, изменяют поверхностные свойства основного металла. В результате металл приобретает высокое электрическое сопротивление. Различные пигменты осуществляют эту реакцию по-разному. Грунтовки поглощают и связывают влагу, чтобы она не вступала в реакцию со сталью.
В результате металл приобретает высокое электрическое сопротивление. Различные пигменты осуществляют эту реакцию по-разному. Грунтовки поглощают и связывают влагу, чтобы она не вступала в реакцию со сталью.
Как выбрать антикоррозионное покрытие
Принимая во внимание следующие критерии, можно определить наиболее эффективный тип антикоррозионного покрытия, необходимого для конкретного проекта.
Качество покрытия/нанесение — Какой уровень антикоррозионной краски необходим? Насколько важно, чтобы краска была устойчивой к выцветанию и/или истиранию? Как часто вы планируете перекрашивать? Есть ли предпочтение нанесения: кисть/валик или распыление?
Эстетика — Какие материалы будут покрыты? Насколько важно, чтобы лакокрасочное покрытие выглядело привлекательно? Важно ли сохранение цвета?
Цена — Как правило, более качественная краска увеличивает цену. Учитываются ли заявки на подкраску при оценке затрат на техническое обслуживание? Какова стоимость выбранной краски? Как часто его нужно будет перекрашивать?
Экологические нормы — Каковы местные экологические нормы для красок и покрытий? Соответствует ли краска этим стандартам? Как процесс покраски повлияет на окружающую среду? С июня 2002 года правительство США введет в действие правила, направленные на снижение количества загрязняющих веществ в краске для повышения защиты окружающей среды. Новые пределы содержания летучих органических соединений (ЛОС) упадут до 450 граммов на литр краски. В Калифорнии, Аризоне, Нью-Йорке и Нью-Джерси последуют более жесткие ограничения, сводящие к минимуму объемы твердых веществ до уровня 340 граммов на литр.
Новые пределы содержания летучих органических соединений (ЛОС) упадут до 450 граммов на литр краски. В Калифорнии, Аризоне, Нью-Йорке и Нью-Джерси последуют более жесткие ограничения, сводящие к минимуму объемы твердых веществ до уровня 340 граммов на литр.
Покрытия
Существует три основных типа покрытий, используемых при ремонтной окраске. В зависимости от качества, цены, применения и эстетических требований операторы установки могут выбрать подходящее покрытие из следующих:
• Алкидные эмали — Алкидные эмали предназначены для внутренних и наружных поверхностей в умеренных и тяжелых условиях. Это покрытие обеспечивает надежную коррозионную стойкость на срок до 3-5 лет. Алкидные эмали обеспечивают глянцевый цвет, устойчивы к выцветанию, могут наноситься кистью, валиком или распылителем. • Эпоксидные покрытия — Эпоксидные покрытия используются для внутренних или наружных поверхностей в промышленных условиях, где сохранение цвета и блеск не важны. Качество покрытия будет лучше, чем у алкидной эмали, так как оно выдерживает суровые промышленные условия. Эпоксидные покрытия лучше всего наносить распылением, но также можно использовать кисти и валики.
Качество покрытия будет лучше, чем у алкидной эмали, так как оно выдерживает суровые промышленные условия. Эпоксидные покрытия лучше всего наносить распылением, но также можно использовать кисти и валики.
• Полиуретановые покрытия — Полиуретановое покрытие является самой качественной краской из всех трех вариантов. Он выдерживает самые суровые условия и может прослужить до 10 лет. Он обеспечивает сильное сохранение цвета и блеска и устойчив к истиранию. Полиуретановые покрытия наносятся методом напыления.
Заключение
Краски работают, потому что они замедляют коррозию, уменьшая скорость тока в процессе электрохимической коррозии. Понимая коррозию, операторы установки могут предсказать, где может возникнуть ржавчина, и распознать факторы окружающей среды на своем предприятии, которые способствуют коррозии. Хорошая новость заключается в том, что, хотя коррозия может быть дорогостоящей, это не обязательно. Краски являются экономически эффективной мерой защиты от коррозии. Регулярное техническое обслуживание, проводимое операторами установки, может свести к минимуму появление и последствия коррозии.
Регулярное техническое обслуживание, проводимое операторами установки, может свести к минимуму появление и последствия коррозии.
Fatima Hussein
24 августа, 2022
сегодня в производственном подкасте
4 августа 2022
Ключевые инфляционные калибра достигают 6,8%, так как цены продолжают расти
июля 29, 2022
, как до конца. Экономическая неопределенность
29 июля 2022 г.
Соглашение с Сенатом должно упростить покупку электромобилей
29 июля 2022 г.
5 коррозионно-стойких металлических покрытий по сравнению с
Легкие металлы стали предпочтительным выбором в широком диапазоне отраслей. Такие металлы, как алюминий, титан и теперь даже магний, стали жизненно важными в автомобильной, аэрокосмической и многих потребительских областях. Сочетание их большого количества, исключительного отношения прочности к весу и универсальности делает их предпочтительным выбором для инженеров по продуктам во всем мире.
Некоторые легкие сплавы обладают превосходной коррозионной стойкостью даже в необработанном виде, но неизбежно, что обработка поверхности будет необходима в готовом изделии для повышения производительности, долговечности и качества. Магний известен своей плохой коррозионной стойкостью, но менее известно, что некоторые алюминиевые сплавы, такие как 2xxx, 7xxx и другие высокопрочные семейства, содержащие медь или другие переходные металлы, также восприимчивы.
Выбор правильного метода защиты от коррозии имеет важное значение для успешного проектирования и производства компонентов. Каждый метод имеет уникальный набор преимуществ и потенциальных проблем. Мы составили это сравнение различных методов лечения, чтобы помочь вам найти наиболее подходящее решение для ваших нужд.
1. Анодирование
Наиболее популярным методом повышения коррозионной стойкости алюминия является анодирование. Вообще говоря, он включает в себя четырехэтапный процесс для достижения защиты.
На первом этапе материал погружают в ванну с проводящим раствором (обычно в ванну с кислотой с низким pH) и соединяют сплав с анодом электрической цепи. При подаче электрического тока на поверхности металла происходит реакция окисления:
2Al (s) + 6OH — (AQ) — 6E — AL 2 O 3 (S) + 3H 2 ON (L) + 3H 2 ON (L) + 2 ON NARTICLE. поверхность металла утолщается, создавая защитный внешний слой из оксида алюминия. Толщина может быть изменена за счет увеличения времени нанесения покрытия, что обеспечивает широкий спектр применения:
- При легком нанесении может обеспечить хорошую предварительную обработку
перед покраской или последующими покрытиями - Особые цветовые эффекты могут быть достигнуты при окрашивании
- При нанесении тонким слоем (обычно <20 мкм) становится полупрозрачным, что
сохраняет металлическую эстетику, при желании
Толщина покрытия играет ключевую роль в определении коррозионной стойкости. В уличных условиях или при интенсивных нагрузках в помещении (например, при постоянном контакте с жидкостью) рекомендуется не менее 20 мкм. Там, где необходима толщина слоев 10 мкм, требуемое более высокое напряжение может повредить материал, растрескивая защитный оксидный слой и становясь пористым.
В уличных условиях или при интенсивных нагрузках в помещении (например, при постоянном контакте с жидкостью) рекомендуется не менее 20 мкм. Там, где необходима толщина слоев 10 мкм, требуемое более высокое напряжение может повредить материал, растрескивая защитный оксидный слой и становясь пористым.
Кроме того, из-за механизма роста и столбчатой микроструктуры на углах широко распространено растрескивание по толщине, что ограничивает защиту краев, обеспечиваемую слоями анодирования. Затворы с горячей водой можно использовать для обеспечения более надежной защиты, но более эффективные уплотнения могут быть достигнуты за счет использования опасных химических растворов, таких как ацетат никеля или дихромат натрия.
В конечном счете, для материалов, которые требуют определенных эстетических качеств, сохраняя при этом высокую коррозионную стойкость при контакте с жидкостями, анодирование не является лучшим методом повышения коррозионной стойкости.
2. ПЭО
Плазменное электролитическое оксидирование (ПЭО) включает использование плазменных разрядов для преобразования металлической поверхности легких металлов. Он образует клейкий оксидный слой, который является твердым и плотным.
Он образует клейкий оксидный слой, который является твердым и плотным.
Компоненты погружаются в ванну, и электрический ток используется для «выращивания» однородного слоя оксида на поверхности. ПЭО происходит в три этапа:
- Окисление подложки (как происходит в процессе анодирования)
- Соосаждение элементов из электролита в покрытие
- Модификация полученного слоя плазменным разрядом
Хотите узнать больше о методологии PEO компании Keronite? Нажмите ниже, чтобы загрузить бесплатный технический документ.
ПЭО образует твердые, плотные и износостойкие покрытия для легких металлов, таких как алюминий, титан и магний. При непосредственном сравнении с анодированными покрытиями ПЭО образует покрытия с более высокой твердостью, химической пассивностью и выгодной нерегулярной структурой пор, которая обеспечивает высокую устойчивость к деформации и более сильную адгезию.
Помимо превосходных физических и химических характеристик, процесс ПЭО можно проводить экологически безопасным методом благодаря доступным для использования безопасным электролитам и нетоксичным побочным продуктам процесса окисления. Электролиты не содержат кислот, аммиака, тяжелых металлов и хрома, в то время как используемые щелочные растворы низкой концентрации малоопасны и легко утилизируются.
Электролиты не содержат кислот, аммиака, тяжелых металлов и хрома, в то время как используемые щелочные растворы низкой концентрации малоопасны и легко утилизируются.
В результате получается гораздо более экологичное решение, чем альтернативы, а также ряд других преимуществ.
3. Хроматное конверсионное покрытие
Усиление государственного и нормативного контроля производственных процессов привело к постепенному отказу от хроматного конверсионного покрытия как метода защиты от коррозии, несмотря на то, что это один из наиболее эффективных методов.
Химические средства конверсии хромата сильно различаются, но многие из них включают применение растворов хромовой кислоты, натрия, хромата или дихромата калия для очистки металлической поверхности вместе с другими добавками. Использование таких добавок вызывает окислительно-восстановительные реакции с поверхностью, оставляя на металле подложки пассивную пленку, содержащую оксид хрома (IV) и гидратированные соединения. Это обеспечивает высокую коррозионную стойкость и хорошо сохраняет последующие покрытия.
Это обеспечивает высокую коррозионную стойкость и хорошо сохраняет последующие покрытия.
Высокая защита от коррозии обусловлена способностью соединений хрома (VI) восстанавливать защитную оксидную пленку на поврежденном участке покрытия при воздействии кислорода воздуха. Это называется самолечением. Аналогичный механизм используется для создания нержавеющей стали: хром, добавленный в сплав, естественным образом образует на поверхности очень тонкий пассивный слой оксида хрома, предотвращающий окисление железа. Это быстро восстанавливается, если поверхность повреждена, а подповерхностный хром подвергается воздействию атмосферы. Хромат также можно использовать в качестве добавки к краскам или в качестве герметика для анодирования, усиливая их защиту от коррозии.
Соединения шестивалентного хрома, используемые в конверсионной обработке хроматом, как теперь известно, однако, обладают повреждающими и канцерогенными свойствами. Побочные продукты хроматных конверсионных покрытий очень опасны, и поэтому неудивительно, что в отношении материалов, использующих этот процесс, проводится жесткая линия.
Сегодня его использование запрещено во многих отраслях промышленности и строго регулируется. Он по-прежнему широко используется в аэрокосмической отрасли, не склонной к риску, но необходимость изменений в этой сфере растет. К сожалению, он остается лучшей химической пассивацией алюминия из-за его свойств самовосстановления. Интенсивные исследования начались в 1980-х, чтобы найти самовосстанавливающиеся альтернативы без хрома, но они еще не соответствуют его общему уровню защиты. Инженеры ищут альтернативы, такие как анодирование или обработка на основе ПЭО, для повышения производительности в суровых условиях.
4. Краски
Растворы для покрытия поверхностей, такие как краски, грунтовки и другие полимерные системы, кажутся безграничными как по наличию, так и по разнообразию. Наиболее привлекательным преимуществом работы с красками является то, что их можно окрашивать, обрабатывать или наносить разными способами.
Полимерные верхние покрытия также доступны в таком разнообразии и способах нанесения. Могут быть сделаны альтернативные химические вещества и добавки, которые обеспечивают такие свойства, как блеск, дополнительную твердость, смазывающую способность, определенные текстуры, температурную стабильность и химическую стойкость, и это лишь некоторые из них.
Могут быть сделаны альтернативные химические вещества и добавки, которые обеспечивают такие свойства, как блеск, дополнительную твердость, смазывающую способность, определенные текстуры, температурную стабильность и химическую стойкость, и это лишь некоторые из них.
Краски представляют собой относительно недорогой метод повышения коррозионной стойкости. Однако задействованные процессы крайне неэффективны; во время нанесения до 50% покрытия может испариться, а при отверждении в печи образуются вредные побочные продукты, которые опасны и дороги в утилизации в больших объемах.
Предлагая отличную химическую и особенно коррозионную стойкость, как и другие полимерные углеводороды, краски мягкие (их твердость оценивается по сравнению с грифелем карандаша), что означает, что они легко царапаются и стираются.
5. Порошковые покрытия
Порошковые покрытия, как и краски, являются еще одним относительно недорогим вариантом. Хотя преимущества порошковых красок почти такие же, как у красок, но более толстые защитные слои можно наносить более эффективно и быстрее.
Покрытия толстые, что добавляет объемные слои (обычно вверх на 80 мкм), которые существенно повышают коррозионную стойкость материала. Платой за эту дополнительную защиту является добавленная толщина, а эстетические эффекты не такие привлекательные и неодинаковые для разных материалов.
Заключение
В этой статье мы попытались дать краткий обзор покрытий из легких материалов для повышения коррозионной стойкости в легких сплавах. На самом деле существуют сотни различных методов и процессов, доступных от разных поставщиков, каждый из которых имеет небольшие вариации в способах достижения результатов.
Выбор правильного покрытия очень важен, но сложен. Используйте целостный взгляд на процесс нанесения покрытия, начиная с ранних стадий проектирования компонентов. Геометрия компонентов, обеспечение подходящего дренажа, избежание несовместимых комбинаций материалов и выбор сплава — все это имеет решающее значение.
Для достижения наилучших результатов выберите предварительную обработку, обеспечивающую хорошую адгезию к основанию и любым последующим обработкам. Верхние покрытия следует выбирать с учетом их совместимости с предварительной обработкой и требуемых свойств конечного использования/функциональных/эстетических свойств.
Верхние покрытия следует выбирать с учетом их совместимости с предварительной обработкой и требуемых свойств конечного использования/функциональных/эстетических свойств.
Защита от коррозии — SteelConstruction.info
Экономичная защита стальных конструкций от коррозии не вызовет затруднений для обычных применений и сред, если с самого начала будут определены факторы, влияющие на долговечность.
Многие стальные конструкции успешно эксплуатируются в течение многих лет даже в неблагоприятных условиях. Первое крупное железное сооружение, мост в Коулбрукдейле, Великобритания, просуществовало более 200 лет, в то время как о железнодорожном мосту Форт, которому более 100 лет, ходят легенды.
Сегодня доступны современные долговечные защитные покрытия, которые при правильном использовании позволяют увеличить интервалы обслуживания и повысить производительность.
Ключ к успеху заключается в распознавании коррозионной активности окружающей среды, воздействию которой будет подвергаться конструкция, и в определении четких и подходящих спецификаций покрытия. Там, где сталь находится в сухом отапливаемом помещении, риск коррозии незначителен, и защитное покрытие не требуется. И наоборот, стальная конструкция, подвергающаяся воздействию агрессивной среды, должна быть защищена высокоэффективной обработкой и, возможно, должна быть спроектирована с учетом технического обслуживания, если требуется продление срока службы.
Там, где сталь находится в сухом отапливаемом помещении, риск коррозии незначителен, и защитное покрытие не требуется. И наоборот, стальная конструкция, подвергающаяся воздействию агрессивной среды, должна быть защищена высокоэффективной обработкой и, возможно, должна быть спроектирована с учетом технического обслуживания, если требуется продление срока службы.
Оптимальная защитная обработка, которая сочетает в себе соответствующую подготовку поверхности, подходящие материалы покрытия, требуемую долговечность и минимальную стоимость, достигается с помощью современной технологии обработки поверхности.
Содержание
- 1 Коррозия конструкционной стали
- 2 Влияние конструкции на коррозию
- 3 Подготовка поверхности
- 4 Лакокрасочные покрытия
- 5 Металлические покрытия
- 5.1 Горячее цинкование
- 5.2 Металлические покрытия, полученные термическим напылением
- 6 Соответствующие спецификации
- 7 Инспекция и контроль качества
- 8 Каталожные номера
- 9 Ресурсы
- 10 Дальнейшее чтение
- 11 См.
 также
также - 12 Внешние ссылки
- 13 CPD
[вверх]Коррозия конструкционной стали
Основная статья: Коррозия конструкционной стали
Схематическое изображение механизма коррозии стали
Коррозия конструкционной стали представляет собой электрохимический процесс, требующий одновременного присутствия влаги и кислорода. При отсутствии того и другого коррозия не возникает. По сути, железо в стали окисляется с образованием ржавчины, которая занимает примерно в 6 раз больше объема исходного материала, потребляемого в процессе. Здесь показан общий процесс коррозии.
Наряду с общей коррозией могут возникать различные виды локальной коррозии; биметаллическая коррозия, точечная коррозия и щелевая коррозия. Однако они, как правило, не имеют существенного значения для металлоконструкций.
Скорость, с которой развивается процесс коррозии, зависит от ряда факторов, связанных с «микроклиматом», непосредственно окружающим конструкцию, в основном от времени увлажнения и уровня загрязнения атмосферы. Из-за изменений в атмосферных условиях данные о скорости коррозии не могут быть обобщены. Тем не менее, среды можно классифицировать в широком смысле, и соответствующие измеренные скорости коррозии стали дают полезный показатель вероятной скорости коррозии. Дополнительную информацию можно найти в BS EN ISO 129.44-2 [1] и BS EN ISO 9223 [2] .
Из-за изменений в атмосферных условиях данные о скорости коррозии не могут быть обобщены. Тем не менее, среды можно классифицировать в широком смысле, и соответствующие измеренные скорости коррозии стали дают полезный показатель вероятной скорости коррозии. Дополнительную информацию можно найти в BS EN ISO 129.44-2 [1] и BS EN ISO 9223 [2] .
| Категория коррозионной активности | Низкоуглеродистая сталь Потеря толщины (мкм) a | Примеры типичных сред (только для справки) | |
|---|---|---|---|
| Внешний вид | Интерьер | ||
| C1 очень низкий | ≤ 1,3 | — | Отапливаемые здания с чистой атмосферой, напр. офисы, магазины, школы, гостиницы |
| C2 низкий | > 1,3 до 25 | Атмосферы с низким уровнем загрязнения: преимущественно сельские районы | Неотапливаемые здания, в которых может образовываться конденсат, напр. склады, спортивные залы склады, спортивные залы |
| C3 средний | > 25 до 50 | Городская и промышленная атмосфера, умеренное загрязнение двуокисью серы; прибрежная зона с низкой соленостью | Производственные помещения с повышенной влажностью и некоторым загрязнением воздуха, напр. предприятия пищевой промышленности, прачечные, пивоварни, молокозаводы |
| C4 высокий | > от 50 до 80 | Промышленные районы и прибрежные районы с умеренным засолением | Химические заводы, плавательные бассейны, прибрежные суда и верфи |
| C5 очень высокий | > 80 до 200 | Промышленные зоны с повышенной влажностью и агрессивной атмосферой и прибрежные зоны с повышенной соленостью | Здания или зоны с почти постоянной конденсацией и высоким уровнем загрязнения |
| CX экстремальный | > 200 до 700 | Морские районы с высокой соленостью и промышленные районы с повышенной влажностью и агрессивной атмосферой, а также субтропические и тропические атмосферы | Промышленные зоны с повышенной влажностью и агрессивной атмосферой |
Примечания:
- 1 мкм (1 микрон) = 0,001 мм
- a Значения потери толщины даны после первого года воздействия.
 Убытки могут уменьшиться в последующие годы.
Убытки могут уменьшиться в последующие годы. - Значения потерь, используемые для категорий коррозионной активности, идентичны значениям, указанным в BS EN ISO 9223 [2] .
[вверх]Влияние конструкции на коррозию
Основная статья: Влияние конструкции на коррозию
Конструкция и детали конструкции могут влиять на долговечность любого нанесенного на нее защитного покрытия. Конструкции, спроектированные с большим количеством мелких конструктивных элементов и крепежных элементов, труднее защитить, чем конструкции с большими плоскими поверхностями. Ключевые вопросы, которые необходимо рассмотреть, включают:
- Доступ для нанесения покрытия и обслуживания
- Избегание ловушек для влаги и мусора
- Предотвращение или герметизация щелей
- Дренаж и вентиляция для минимизации времени увлажнения
- Тщательное управление контактом с другими материалами
Общие указания по предотвращению коррозии за счет надлежащей детализации конструкции можно найти в BS EN ISO 12944-3 [3] , а также некоторые типичные рекомендации и запреты для стальных каркасов. здания показаны ниже.
здания показаны ниже.
Примеры детализации зданий
[вверх]Подготовка поверхности
Основная статья: Подготовка поверхности
Стальная балка, выходящая из установки автоматической пескоструйной очистки
Подготовка поверхности — это обязательный первый этап обработки стальной подложки перед нанесением любого покрытия, который обычно считается наиболее важным фактором, влияющим на общий успех защиты от коррозии система.
Характеристики покрытия в значительной степени зависят от его способности должным образом прилипать к материалу подложки. Исходное состояние поверхности стали может варьироваться в зависимости от количества остаточной прокатной окалины и степени начальной ржавчины. Однако, как правило, это неудовлетворительная основа для нанесения современных высокоэффективных защитных покрытий. Существует ряд методов подготовки и степеней чистоты, но, безусловно, наиболее важным и важным методом, используемым для тщательной очистки поверхностей от прокатной окалины и ржавчины, является абразивоструйная очистка. Стандартные степени чистоты для абразивоструйной очистки в соответствии с ISO 8501-1 [4] являются:
Стандартные степени чистоты для абразивоструйной очистки в соответствии с ISO 8501-1 [4] являются:
- Sa 1 – Легкая пескоструйная очистка
- Sa 2 – Тщательная пескоструйная очистка
- Sa 2½ – Очень тщательная пескоструйная очистка
- Sa 3 – Дробеструйная очистка до визуально чистой стали
Ручная пескоструйная очистка
(Видео предоставлено Corrodere/MPI)
Процесс подготовки поверхности не только очищает сталь, но также обеспечивает подходящий профиль и амплитуду поверхности для нанесения защитного покрытия. Толстослойные лакокрасочные покрытия и металлические покрытия, полученные термическим напылением, требуют грубого угловатого профиля поверхности для обеспечения механического ключа. Это достигается за счет использования абразивных материалов. Дробеструйные абразивы используются для тонкопленочных лакокрасочных покрытий, таких как заводские грунтовки. Разница между дробью и дробью и соответствующими профилями поверхности показана ниже на трехмерных диаграммах, полученных с помощью оборудования для бесконтактного определения характеристик поверхности.
Дробеструйные абразивы используются для тонкопленочных лакокрасочных покрытий, таких как заводские грунтовки. Разница между дробью и дробью и соответствующими профилями поверхности показана ниже на трехмерных диаграммах, полученных с помощью оборудования для бесконтактного определения характеристик поверхности.
Абразивная дробь
Зернистый абразив
После абразивоструйной очистки можно проверить дефекты поверхности и изменения поверхности, возникшие в процессе изготовления, например. сварка. Некоторые поверхностные дефекты, появившиеся во время первоначальной обработки стали, могут не оказывать отрицательного влияния на эксплуатационные характеристики покрытия, особенно для конструкций в категориях окружающей среды с относительно низким уровнем риска. Однако, в зависимости от конкретных требований к конструкции, может потребоваться дополнительная обработка поверхности для удаления поверхностных дефектов на сварных швах и кромках реза, а также растворимых солей, чтобы обеспечить приемлемое состояние поверхности для окраски.
[вверх]Лакокрасочные покрытия
Основная статья: Лакокрасочные покрытия
Поперечное сечение многослойной системы окраски
Лакокрасочные покрытия для стальных конструкций разрабатывались на протяжении многих лет в соответствии с промышленным законодательством по защите окружающей среды и в ответ на требования владельцев мостов и сооружений о повышении долговечности. Краска состоит из пигмента, диспергированного в связующем и растворенного в растворителе. Наиболее распространены методы классификации красок либо по их пигментации, либо по типу связующего вещества.
Современная система окраски обычно включает последовательное нанесение красок или, альтернативно, красок, наносимых поверх металлических покрытий, для образования «дуплексной» системы покрытия. Защитные лакокрасочные системы обычно состоят из грунтовки, промежуточных/сборочных слоев и финишных слоев. Каждый «слой» покрытия в любой защитной системе выполняет определенную функцию, и различные типы наносятся в определенной последовательности: грунтовка, промежуточные/сборочные слои в цеху и, наконец, финишное покрытие (или верхнее покрытие) либо в цехе. или на месте.
или на месте.
Предварительные грунтовки используются на металлоконструкциях сразу после пескоструйной очистки, чтобы сохранить реактивно очищенную поверхность в состоянии отсутствия ржавчины в процессе изготовления до тех пор, пока не будет проведена окончательная покраска. Эти типы грунтовки не используются перед нанесением термического напыления покрытий.
Способ нанесения систем окраски и условия нанесения оказывают существенное влияние на качество и долговечность покрытия. Стандартные методы, используемые для нанесения красок на стальные конструкции, включают нанесение кистью, валиком, обычным воздушным распылением и безвоздушным распылением/электростатическим безвоздушным распылением.
Безвоздушное распыление стало наиболее часто используемым методом нанесения лакокрасочных покрытий на стальные конструкции в контролируемых заводских условиях. нанесение кистью и валиком чаще используется для нанесения на месте, хотя также используются методы распыления. Покрытия «полосатые», наносимые на кромки и острые углы, обычно наносятся кистью.
- Безвоздушное распыление на стальные балки мостов
Основными условиями, влияющими на нанесение лакокрасочных покрытий, являются температура стали и окружающей среды, а также влажность. Их легче контролировать в условиях магазина, чем на месте. С появлением современных высокоэффективных покрытий правильное нанесение становится все более важным для достижения намеченных характеристик. Промышленность признала это и ввела схему обучения и сертификации специалистов по нанесению красок (ICATS — Схема обучения специалистов по нанесению покрытий). Регистрация ICATS (или эквивалентная схема, например, Trainthepainter) впоследствии стала обязательным требованием для работы на мостах Highways England и сооружениях Network Rail.
Безвоздушное распыление краски
(Видео предоставлено Corrodere/MPI)
[вверх]Металлические покрытия
Основная статья: Металлические покрытия
Существует четыре широко используемых метода нанесения металлического покрытия на стальные поверхности. Это горячее цинкование, термическое напыление, гальваническое покрытие и шерардизация. Последние два процесса не используются для металлоконструкций, но используются для фитингов, крепежных изделий и других мелких предметов. В целом защита от коррозии, обеспечиваемая металлическими покрытиями, в значительной степени зависит от выбора металла покрытия и его толщины и не сильно зависит от способа нанесения.
Это горячее цинкование, термическое напыление, гальваническое покрытие и шерардизация. Последние два процесса не используются для металлоконструкций, но используются для фитингов, крепежных изделий и других мелких предметов. В целом защита от коррозии, обеспечиваемая металлическими покрытиями, в значительной степени зависит от выбора металла покрытия и его толщины и не сильно зависит от способа нанесения.
[вверх]Горячее цинкование
Стальные элементы, извлекаемые из обычной ванны для горячего цинкования
Горячее цинкование — это процесс, который включает погружение стального компонента, подлежащего покрытию, в ванну с расплавленным цинком (при температуре около 450 °C) после травления и флюсования, а затем отзыв его. Погруженные поверхности равномерно покрыты цинковым сплавом и слоями цинка, образующими металлургическую связь с подложкой. Полученное покрытие является прочным, прочным, устойчивым к истиранию и обеспечивает катодную (жертвенную) защиту любых небольших поврежденных участков на стальной основе. Типичная минимальная средняя толщина покрытия для стальных конструкций составляет 85 мкм.
Типичная минимальная средняя толщина покрытия для стальных конструкций составляет 85 мкм.
Поперечное сечение горячеоцинкованного покрытия
[вверх] Металлические покрытия термическим напылением
Поперечный разрез термически напыленного алюминиевого покрытия
Термически напыленные покрытия из цинка, алюминия и цинко-алюминиевых сплавов могут обеспечить долговременную защиту от коррозии стальных конструкций, подвергающихся воздействию агрессивных сред. Металл в виде порошка или проволоки подается через специальный пистолет-распылитель, содержащий источник тепла, которым может быть кислородное пламя или электрическая дуга. Капли расплавленного металла выдуваются струей сжатого воздуха на предварительно очищенную пескоструйным методом стальную поверхность. Легирования не происходит, покрытие состоит из перекрывающихся пластин металла и является пористым. Затем поры герметизируются путем нанесения тонкого органического покрытия, проникающего вглубь поверхности. Важно, чтобы герметик полностью заполнил все поры в металлическом покрытии.
Важно, чтобы герметик полностью заполнил все поры в металлическом покрытии.
Адгезия напыленных металлических покрытий к стальным поверхностям считается в основном механической по своей природе. Поэтому необходимо наносить покрытие на чистую шероховатую поверхность, и обычно рекомендуется пескоструйная очистка крупнозернистым абразивом.
Дуговое напыление
(Видео предоставлено Metallisation)
[вверх]Подходящие спецификации
Основная статья: Подходящие спецификации
Общий успех схемы защитного покрытия начинается с хорошо подготовленной спецификации. Это важный документ, предназначенный для предоставления подрядчику четких и точных инструкций о том, что и как следует делать. Спецификация должна быть составлена кем-то с соответствующими техническими знаниями, и в ней должно быть ясно, что требуется, а что является практичным и достижимым.
Он должен быть написан в логической последовательности, начиная с подготовки поверхности, проходя через каждую наносимую краску или металлическое покрытие и, наконец, касаясь конкретных областей, например. сварные швы. Он также должен быть максимально кратким, согласующимся с предоставлением всей необходимой информации. Наиболее важными элементами спецификации являются следующие:
- Обработка металла для удаления острых краев, выступов и т. д., а также стальных загрязнений.
- Метод подготовки поверхности и требуемый стандарт.
- Максимальный интервал между подготовкой поверхности и последующим грунтованием или металлическим покрытием.
- Типы используемых красок или металлических покрытий, поддерживаемые соответствующими стандартами.
- Используемый(е) метод(ы) применения.
- Количество наносимых слоев и интервал между слоями.
- Толщина влажной и сухой пленки для каждого слоя.
- Место, где должен наноситься каждый слой (т.
 е. магазины или строительная площадка), и требуемые условия нанесения с точки зрения температуры, влажности и т. д.
е. магазины или строительная площадка), и требуемые условия нанесения с точки зрения температуры, влажности и т. д. - Детали для обработки сварных швов, болтовых соединений и т. д.
- Процедуры устранения повреждений и т. д.
Большинство стальных мостов защищены в соответствии с требованиями Highways England и стандартными спецификациями Network Rail. Для других мостов могут быть указаны альтернативные системы и методы покрытия, но должны применяться те же стандарты и принципы надлежащей практики покрытия.
[вверх]Инспекция и контроль качества
Основная статья: Инспекция и контроль качества
Ассортимент приборов для испытаний и контроля
Контроль является неотъемлемой частью контроля качества. Его целью является проверка соблюдения требований спецификации и предоставление клиенту отчета с надлежащими записями. Одним из самых больших преимуществ для инспектора по покрытиям является четкая письменная спецификация, на которую можно без сомнений ссылаться.
Назначение стороннего инспектора с соответствующей квалификацией следует рассматривать как инвестиции в качество, а не просто как дополнительные расходы. Проверка процессов, процедур и материалов, необходимых для нанесения защитного покрытия на стальные конструкции, имеет жизненно важное значение, поскольку серьезную ошибку даже в одной операции нельзя легко обнаружить после выполнения следующей операции, и если ее не исправить немедленно, это может значительно снизить ожидаемые срок службы до первого технического обслуживания.
[наверх]Ссылки
- ↑ 1.0 1.1 BS EN ISO 12944-2: 2017, Краски и лаки. Защита стальных конструкций от коррозии системами защитной окраски. Часть 2. Классификация сред, BSI
- ↑ 2.0 2.1 BS EN ISO 9223: 2012, Коррозия металлов и сплавов. Коррозионная активность атмосферы. Классификация, определение и оценка BSI
- ↑ BS EN ISO 12944-3: 2017, Краски и лаки. Защита стальных конструкций от коррозии защитными системами окраски.
 Часть 3. Вопросы проектирования, BSI
Часть 3. Вопросы проектирования, BSI - ↑ BS EN ISO 8501-1: 2007 Подготовка стальных поверхностей перед нанесением красок и сопутствующих продуктов. Визуальная оценка чистоты поверхности. Степени ржавчины и степени подготовки стальных поверхностей без покрытия и поверхностей после полного удаления предыдущих покрытий, ISO
Ресурсы
- Хенди, Ч.Р.; Айлс, округ Колумбия (2015) Группа стальных мостов: Руководящие указания по передовой практике строительства стальных мостов (6-й выпуск). (стр. 185). SCI
- Руководство 8.01 Подготовка к эффективной защите от коррозии
- Руководство 8.02 Защитная обработка крепежных изделий
- Руководство 8.03 Горячее цинкование погружением
- Руководство 8.04 Металлические покрытия, полученные термическим напылением
- Руководство 8.05 Высокоэффективные лакокрасочные покрытия
- Руководство 8.06 Проверка подготовки поверхности и обработки покрытий
- Стальные здания, 2003 г.
 , Британская ассоциация строительных металлоконструкций, ООО.
, Британская ассоциация строительных металлоконструкций, ООО.- Глава 12 – Защита от коррозии
[наверх]Дополнительная литература
- Д.Дикон и Р.Хадсон (2012 г.), Руководство по проектированию металлоконструкций (7-е издание), глава 36 – Коррозия и предотвращение коррозии, Институт стальных конструкций.
- Д.А. Bayliss & D.H.Deacon (2002), Steelwork Corrosion Control (2-е издание), Spon Press
[вверху] См. также
- Коррозия конструкционной стали
- Влияние конструкции на коррозию
- Подготовка поверхности
- Лакокрасочные покрытия
- Стандартные системы защиты зданий от коррозии
- Металлические покрытия
- Соответствующие спецификации
- Инспекция и контроль качества
[наверх]Внешние ссылки
- Британская федерация покрытий
- Ассоциация гальванистов
- Ассоциация исследований красок
- Ассоциация термического напыления и обработки поверхностей
- ИКАТС
- Корродор
- Защита от коррозии
Предотвращение коррозии металла |
Зачем беспокоиться о предотвращении коррозии металла? Коррозия металла – серьезная проблема. Ежегодные затраты на коррозию во всем мире составляют 2,2 трлн долларов США, что составляет более 3% мирового ВВП.
Ежегодные затраты на коррозию во всем мире составляют 2,2 трлн долларов США, что составляет более 3% мирового ВВП.
Когда возникает коррозия, она представляет реальную угрозу конструкциям. Могут быть затронуты здания, дороги и мосты, а это означает, что коррозия металла ставит под угрозу безопасность населения.
Предотвращение коррозии металлов является важной задачей, поскольку это не только экономит деньги, но и спасает жизни.
В этой статье объясняется, что такое коррозия, как она возникает, как лучше всего предотвратить коррозию металла и как защитить свою тяжелую работу.
Чтобы получить современную отделку, обеспечивающую непревзойденную коррозионную стойкость в самых суровых условиях, свяжитесь с нами по адресу https://minnesotaindustrialcoatings.com/
Что такое коррозия металлов?
Проще говоря, коррозия металла — это процесс, при котором металл взаимодействует с окружающей средой, такой как воздух и вода, и разрушается.
Скорость и степень этого износа зависят от нескольких факторов, включая тип металла и условия окружающей среды.
Для возникновения коррозии металла необходимы три условия. Это влага, открытая металлическая поверхность и окислитель.
При коррозии железа и стали образующийся оксид широко известен как ржавчина.
Есть несколько способов минимизировать коррозию.
Некоторые металлы более подвержены коррозии?
Некоторые металлы более подвержены коррозии, чем другие, например, чистое железо. Но все металлы подвержены тому или иному типу коррозии металла.
Ржавчина — это особый тип коррозии или окисления, который возникает только у черных металлов (содержащих железо).
Некоторыми часто используемыми черными металлами являются углеродистая сталь, легированная сталь и нержавеющая сталь. Другие металлы, не содержащие железа, могут подвергаться коррозии, но не ржаветь.
Предотвращение коррозии металла начинается с выбора подходящего металла. Некоторые металлы более устойчивы к коррозии. Например, нержавеющая сталь (сочетание стали с железом и другими сплавами) подвержена значительно более медленной коррозии.
Хотя сплавы нержавеющей стали содержат железо, они устойчивы к ржавчине, поскольку содержат высокий процент хрома. Хром очень быстро окисляется и создает слой оксида хрома на поверхности металла. Таким образом, он предотвращает попадание кислорода в сталь под ним.
Небольшая группа благородных металлов, обладающих сверхстойкостью к коррозии, включает золото, серебро, платину, родий и палладий.
Почему или как возникает коррозия?
Коррозия вызывается средой, окружающей металл. Это результат химической реакции, которая происходит, когда металл реагирует с окружающими жидкостями и газами.
Как отмечалось ранее, для коррозии стали необходима влага. Следовательно, для коррозии стали необходим электролит, а многие электролиты представляют собой растворы в воде или каком-либо другом растворителе. Ржавчина возникает, когда железо подвергается воздействию дождя и влаги в воздухе, соленой воде, кислотах или других агрессивных химикатах. Металл и влага реагируют с кислородом и образуют ржавчину.
Вот почему сталь медленнее корродирует в сухом климате. Однако во влажном и дождливом климате защита стали имеет жизненно важное значение. Следующие среды усугубляют процесс коррозии:
Коррозия в промышленных зонах происходит быстрее из-за кислот, щелочей и других химических веществ, содержащихся в дыме и других испарениях.
Соленая вода разъедает сталь быстрее, чем пресная. Именно поэтому районы вблизи океана особенно опасны из-за воздействия соленого воздуха.
Подземные трубы также особенно подвержены коррозии, поскольку глина и почва являются хорошими проводниками электричества.
Есть ли способ предотвратить коррозию металла?
Коррозия металла — это реальность, с которой приходится сталкиваться каждому, кто использует металл. Знание причин коррозии — это первый шаг к пониманию того, что можно сделать для ее предотвращения.
Мы знаем, что для коррозии необходимы три вещи: электролит, открытый металл и акцептор электронов (воздух).
Коррозию металлов можно предотвратить, эффективно устранив одно из этих условий.
Например, покрытие металлической поверхности создает барьер между металлом и влагой окружающей среды.
Давайте теперь рассмотрим этот метод покрытия металлов для предотвращения коррозии и другие более подробно.
Как можно предотвратить коррозию металлов?
Вот несколько общих способов предотвращения коррозии:
- Техническое обслуживание
- Принять меры по изменению окружающей среды
- Использовать жертвенное покрытие
- Использовать защитное покрытие
Техническое обслуживание
7 90 интенсивный, но эффективный способ замедлить разрушительное воздействие коррозии. Во-первых, вы можете физически соскоблить ржавчину как можно быстрее после ее появления. Затем удалите его старым добрым методом очистки с мылом и водой.
Экологические меры
Окружающая среда является основной причиной коррозии. Поэтому логически, если вы можете контролировать эту среду, вы можете снизить риск коррозии.
В качестве простого примера рассмотрим очистку воды в водогрейных котлах. Обработка изменяет такие факторы, как жесткость, щелочность или содержание кислорода. В результате металл, который вступает в контакт с этой водой, будет иметь меньшую скорость коррозии.
Жертвенные покрытия
Временное покрытие относится к одному из методов покрытия металлов для предотвращения коррозии. Покрытие металлической поверхности другим металлом, который с большей вероятностью окисляется, защищает базовый слой.
Например, сталь часто покрывают цинком, который легче окисляется. Цинк «приносится в жертву» для защиты железа в стали. Этот тип защиты называется «катодной защитой», также известной как цинкование.
Другим способом защиты металла является «анодная защита». Это включает нанесение покрытия из менее легко окисляемого металла, такого как олово.
Используйте защитное покрытие
Одним из наиболее эффективных способов предотвращения коррозии и ржавчины является защита металлоконструкций промышленными покрытиями. Покрытие металлов краской или эмалью для предотвращения гниения является высокоэффективным методом. Он создает барьер между металлом и влагой и кислородом окружающей среды.
Покрытие металлов краской или эмалью для предотвращения гниения является высокоэффективным методом. Он создает барьер между металлом и влагой и кислородом окружающей среды.
Чем выше качество покрытия, тем выше защита. Minnesota Industrial Coatings (MIC) поставляет неизменно высококачественные промышленные покрытия, в том числе порошковые и гальванопокрытия.
Мы являемся одной из немногих компаний, которые могут предложить как порошковое покрытие, так и электронное покрытие. Таким образом, при совместном использовании (основа E-coat с верхним покрытием Powder) вы получаете лучшее из обоих миров.
В результате получается качественная отделка, множество вариантов цвета и непревзойденная коррозионная стойкость даже в самых суровых условиях.
Да, коррозия металла — серьезная проблема. Защитите свою работу с помощью наилучшей коррозионной стойкости, химической стойкости, устойчивости к царапинам, стойкости к сколам и износоустойчивой поверхности.
Чтобы запросить оценку, свяжитесь с нами сегодня!
Порошковое покрытие против цинкования: когда использовать одно, другое или оба
Миннесота Промышленные покрытия
29 августа 2022 г.
Когда дело доходит до защиты металла, существует несколько вариантов создания защитного антикоррозионного слоя. Коррозия может испортить любую стальную конструкцию, начиная от стали…
Подробнее »
Когда наносить порошковое покрытие на нержавеющую сталь
Миннесота Промышленные покрытия
9 июля 2022 г.
Нержавеющая сталь — отличный материал для многих интерьеров и экстерьеров зданий. Нержавеющий элемент представляет собой смесь сплавов, которые делают сталь…
Подробнее »
Состав для защиты от коррозии — Центр знаний Prospector
Поделитесь этой статьей:
Коррозия — это процесс, при котором металл может разлагаться в результате электрохимических и/или химических процессов. Металлы стремятся находиться в своем наиболее термодинамически стабильном состоянии, которое, упрощенно говоря, является естественным состоянием вещества в его самом низком энергетическом состоянии. Металлы обычно существуют в природе в виде оксидов (например, оксид железа, оксид алюминия, оксид цинка, поскольку оксиды представляют их самое низкое энергетическое состояние). Поскольку коррозия обычно ускоряется в присутствии воды, кислорода и солей (особенно сильных кислот), функция системы защитного покрытия состоит в том, чтобы максимально защитить металлическую основу от этих сил.
Металлы обычно существуют в природе в виде оксидов (например, оксид железа, оксид алюминия, оксид цинка, поскольку оксиды представляют их самое низкое энергетическое состояние). Поскольку коррозия обычно ускоряется в присутствии воды, кислорода и солей (особенно сильных кислот), функция системы защитного покрытия состоит в том, чтобы максимально защитить металлическую основу от этих сил.
Окисление происходит на аноде (положительный электрод), а восстановление происходит на катоде (отрицательный электрод). Коррозия обычно ускоряется в присутствии воды, кислорода и солей (особенно солей сильных кислот).
Процесс коррозии в случае стали (рис. 1 и 2) ниже.
В данной статье будет рассмотрено влияние следующих формулирующих факторов на коррозионную стойкость покрытия.
- Тип металла
- Уровень пигмента и выбор
- Пигменты, замедляющие коррозию
- Вопросы среды обслуживания и новые инновации
1.
 Тип металла
Тип металла
Согласно серии ЭМП алюминий и цинк более активны, чем железо, и быстрее окисляются при воздействии кислорода и воды. Однако оксиды непокрытого цинка и алюминия образуют прочно связанный слой с поверхностью металла, что снижает скорость коррозии нижележащего металла. Тогда как при ржавчине углеродистой стали продуктом коррозии является оксид железа, который слабо прикреплен к поверхности, склонной к более быстрому окислению.
В серии EMF (рис. 3 ниже) Zn более активен, чем Fe. Когда грунтовка с высоким содержанием цинка наносится на сталь или в случае оцинкованной стали, цинк окисляется преимущественно до стали и, таким образом, предотвращает окисление нижележащей стали. В этом сценарии Zn является анодным (более легко окисляется) по отношению к стали и, следовательно, защищает сталь от окисления. Таким образом, сталь защищена от коррозии катодным ингибированием, а также барьером, который обеспечивает грунтовка с высоким содержанием цинка.
Рисунок 3
2.
 Соображения по пигментам
Соображения по пигментам
PVC (объемная концентрация пигмента) в системе определяется как объемный процент твердых частиц в системе после образования пленки, когда все летучие ингредиенты, такие как растворители и вода, испарились. Уровень и тип пигмента, используемого в грунтовке, влияет не только на начальную адгезию покрытия, но и на его долговечность в процессе эксплуатации. Состав большинства грунтовок соответствует критической объемной концентрации пигмента (CPVC) или немного ниже, чтобы максимизировать адгезию верхнего слоя (более шероховатая поверхность грунтовки и более высокая свободная энергия), а также многие другие свойства покрытия (рис. 4).
Рисунок 4 – Влияние ХПВХ на свойства покрытия
ПВХ и взаимосвязь между ПВХ и критической объемной концентрацией является важным фактором, который определяет не только механические свойства, но также влияет на проникновение влаги и кислорода через пленку покрытия к металлической подложке. В зависимости от области применения и требуемых механических свойств (например, адгезия к подложке, гибкость, адгезия к верхнему слою, способность к шлифованию) коррозионно-стойкие грунтовки изготавливаются для различных видов ПВХ и содержат различные инертные пигменты.
Использование более полярных пигментов может обеспечить легкое смачивание в процессе диспергирования пигмента, но может ухудшить долговременную адгезию, поскольку они более восприимчивы к миграции влаги и отслоению на границе покрытия и подложки. Пластинчатые пигменты и пигменты с очень низким содержанием водорастворимых компонентов или вообще без них также продлевают срок службы.
Размер, форма и структура частиц пигмента могут влиять на проникновение влаги и кислорода и, в конечном счете, на коррозионную стойкость. Пигменты с пластинчатыми частицами могут снижать проницаемость, особенно если они расположены параллельно поверхности покрытия. Слюда, слюдяной оксид железа и металлические чешуйки являются несколькими примерами таких пигментов. Эти пластинчатые пигменты обеспечивают более мучительный путь воды, растворимых солей и кислорода для достижения поверхности металла. Другие пигменты, которые способствуют коррозионной стойкости, включают силикат алюминия Platy и волластонит (силикат кальция).
3. Пигменты, замедляющие коррозию
Как указано выше, ПВХ и выбор инертных пигментов влияют на барьерные свойства покрытия и повышают коррозионную стойкость. C пигменты, ингибирующие коррозию влияют на скорость коррозии двумя основными механизмами: катодным и анодным ингибированием. Катодное ингибирование подавляет коррозию, препятствуя потоку электронов на катоде, тогда как анодное ингибирование ингибирует коррозию, препятствуя потоку электронов на аноде.
При выборе антикоррозионного пигмента необходимо учитывать несколько факторов. Факторы окружающей среды, влияющие на скорость коррозии, включают влажность, рН влаги, влажные и сухие циклы, растворимые соли, температуру и время. Имея в виду эти проблемы, необходимо тщательно продумать критерии оценки и методы испытаний, прежде чем выбирать пигменты, ингибирующие коррозию. Ингибирующие коррозию или пассивирующие пигменты способствуют образованию барьерного слоя над анодными областями, тем самым пассивируя поверхность. Чтобы быть эффективными, эти пигменты имеют минимальную растворимость. Если растворимость слишком высока, пигмент будет слишком быстро выщелачиваться из покрытия, что сократит время, в течение которого пигмент будет доступен для подавления коррозии. Если пленка покрытия более открытая (например, воздушно-сухой латекс), водопроницаемость выше, и, таким образом, ингибирующий коррозию пигмент будет истощаться быстрее. Для правильного функционирования покрытие должно допускать диффузию некоторого количества воды для растворения пигмента. Соответственно, образование пузырей может происходить во влажных условиях по мере растворения пигмента. Известно, что связующие с более высокой Tg (температурой стеклования) и более высокой плотностью поперечных связей улучшают устойчивость к образованию пузырей.
Чтобы быть эффективными, эти пигменты имеют минимальную растворимость. Если растворимость слишком высока, пигмент будет слишком быстро выщелачиваться из покрытия, что сократит время, в течение которого пигмент будет доступен для подавления коррозии. Если пленка покрытия более открытая (например, воздушно-сухой латекс), водопроницаемость выше, и, таким образом, ингибирующий коррозию пигмент будет истощаться быстрее. Для правильного функционирования покрытие должно допускать диффузию некоторого количества воды для растворения пигмента. Соответственно, образование пузырей может происходить во влажных условиях по мере растворения пигмента. Известно, что связующие с более высокой Tg (температурой стеклования) и более высокой плотностью поперечных связей улучшают устойчивость к образованию пузырей.
Подавляющее большинство пигментов, ингибирующих коррозию, состоят из комбинации ионов металлов (катионов), полученных из цинка, стронция, хрома, свинца, молибдена, алюминия, кальция или бария, и анионов, например, полученных из фосфорных (ортофосфорных и полифосфорных кислоты), хромовая кислота и борная кислота. Хотя хромат и свинец, содержащие пассивирующие пигменты, очень эффективно ингибируют коррозию, их использование очень ограничено из-за множества экологических и токсикологических норм.
Хотя хромат и свинец, содержащие пассивирующие пигменты, очень эффективно ингибируют коррозию, их использование очень ограничено из-за множества экологических и токсикологических норм.
Другим важным фактором при выборе пигмента, ингибирующего коррозию, является рН. Например, пигмент с высоким pH может оказывать вредное воздействие на отверждение кислотно-катализируемых систем. И наоборот, пигмент с низким pH может отрицательно сказаться на стабильности систем на водной основе.
4. Условия эксплуатации, соображения и новые инновации
Относительная коррозионная стойкость покрытий может значительно различаться в зависимости от метода испытания и условий воздействия. Общие методы испытаний включают солевой туман (95 % влажности/5 % соли и всегда во влажном состоянии), кислотный солевой туман, циклическая коррозия прогезии (влажный и сухой цикл с 0,04 % сульфата аммония и 0,05 % соли), спектроскопия электрохимического импеданса и солевая пропитка. Большинство экспертов сходятся во мнении, что ускоренные испытания не всегда являются хорошим индикатором того, как металл с покрытием будет вести себя в реальных условиях.
Дополнительными соображениями являются тип металла (например, сталь, алюминий, оцинкованный), предварительная обработка и чистота поверхности. Если металлическая поверхность не очищена и не подготовлена должным образом, покрытие не будет иметь достаточной адгезии, что приведет к преждевременному выходу из строя.
Кроме того, тип покрытия, в котором будут использоваться пигменты, влияет на выбор соответствующих антикоррозионных пигментов. Соображения включают в себя, является ли покрытие на основе растворителя, на водной основе, порошковым, воздушно-сухим или запеченным, а также будет ли пленка сшитой или термопластичной.
Другие факторы, влияющие на коррозию подложки, включают степень гидрофобности покрытия. Поверхностная и объемная гидрофобность может быть увеличена за счет использования модификаторов поверхности специально разработанных/структурированных пигментов, а также добавления гидрофобных добавок, которые минимизируют проникновение влаги в покрытие и, таким образом, снижают скорость коррозии.
Рисунок 5
Наш опыт показывает, что покрытие с высоким контактным углом и объемной гидрофобностью также обеспечивает превосходное сохранение адгезии после ускоренных испытаний, таких как соляной туман или конденсационная влажность.
Рисунок 6
Двухкомпонентный полиэфир-уретан с углом контакта 155 градусов и отличной объемной гидрофобностью, разработанный в лаборатории Chemical Dynamics, LLC
Выборка поставщиков антикоррозионных пигментов включает:
- Buckman
- Грейс
- Галокс (ЕС)
- Хойбах (ЕС)
- Нубиола (ЕС)
- SNCZ (ЕС)
Prospector — это ведущий ресурс для специалистов по разработке лакокрасочных материалов. Найдите нужные материалы и рецептуры в быстром поиске. Зарегистрируйте бесплатную учетную запись сегодня!
Статьи по теме
Статьи «Краски и покрытия»:
- Концентрация пигмента по объему – часть I, автор Jochum Beetsma
- Влияние объемной концентрации пигмента на свойства покрытий – Часть II, Рон Леварчик
- Понимание антикоррозионных пигментов Рона Леварчика
- Инертные пигменты — невидимый вклад в улучшение характеристик краски, Рон Леварчик
- На поверхности: разработка гидрофобных покрытий для прорыва производительности, Рон Леварчик
- Руководство по обеспечению идеальной адгезии покрытия Рона Леварчика
.




 При воздействии с кислыми почвами процесс коррозии наблюдается наиболее агрессивно. Грунты с песком воздействуют медленней всего.
При воздействии с кислыми почвами процесс коррозии наблюдается наиболее агрессивно. Грунты с песком воздействуют медленней всего. д.
д. также
также Убытки могут уменьшиться в последующие годы.
Убытки могут уменьшиться в последующие годы. е. магазины или строительная площадка), и требуемые условия нанесения с точки зрения температуры, влажности и т. д.
е. магазины или строительная площадка), и требуемые условия нанесения с точки зрения температуры, влажности и т. д.