Содержание
схемы доработки кислотной батареи, время, когда подключить зарядное устройство, и как правильно заряжать током?
Содержание
- 1 Тип и режим работы кислотной АКБ с напряжением 12 В
- 2 Как правильно заряжать свинцовую аккумуляторную батарею?
- 3 Правила зарядки аккумуляторной батареи автомобиля
- 3.1 Постоянным током
- 3.2 Постоянным напряжением
- 4 Когда это нужно делать?
- 5 Как влияет температура на процесс?
- 6 Обязательно ли снимать АКБ с машины, прежде чем подключить к устройству?
- 7 Какие есть особенности у зарядного устройства?
- 8 Схема доработки
- 8.1 Выбор выходного напряжения
- 8.2 Добавление светодиода зеленого цвета и резистора r4 параллельно оптрону
- 8.3 Добавление петли гистерезиса ограничения тока
Многие считают, что для того, чтобы зарядить кислотно-свинцовый аккумулятор, достаточно обратиться к заводским инструкциям. Но на самом деле ни один документ не сможет предложить достаточную и полную информацию для осуществления зарядки: условия, применяемые средства и время. Для того, чтобы решить этот вопрос, необходимо использовать дополнительные источники информации.
Для того, чтобы решить этот вопрос, необходимо использовать дополнительные источники информации.
Тип и режим работы кислотной АКБ с напряжением 12 В
Для начала необходимо определить класс батареи, работа которой строится на реакции свинца и серной кислоты между собой. Это делается для того, чтобы выявить алгоритм зарядки для конкретной АКБ. По теории каждый свинцовый аккумулятор имеет два режима зарядки:
- Буферный. Заряжается от сети, редко производит самостоятельную зарядку.
- Циклический. Зарядка происходит сменой циклов, состоящих из разрядки-подзарядки.
К SLA-аккумуляторам преимущественно относятся автомобильные аккумуляторы классического типа. Среди АКБ, которые используются в велобайках и другом индивидуальном электротранспорте, числятся гелевые, буферные, герметичные и необслуживаемые свинцово-кислотные источники тока.
Как правильно заряжать свинцовую аккумуляторную батарею?
Для того, чтобы восстановить затраченную ёмкость, необходимо зарядить свинцовый аккумулятор. Заряженная свинцовая аккумуляторная батарея всегда будет исправно работать, если в автомобиле исправен генератор и машина постоянно используется, если же мощность для источника энергии потеряна, то ее можно вернуть, если воспользоваться специальным устройством для зарядки кислотной АКБ при номинальном напряжении в 12 В.
Заряженная свинцовая аккумуляторная батарея всегда будет исправно работать, если в автомобиле исправен генератор и машина постоянно используется, если же мощность для источника энергии потеряна, то ее можно вернуть, если воспользоваться специальным устройством для зарядки кислотной АКБ при номинальном напряжении в 12 В.
Правила зарядки аккумуляторной батареи автомобиля
Для того, чтобы зарядить АКБ, необходимо следовать простым правилам:
- устройство должно быть установлено только на ровную поверхность;
- без строгого соблюдения полярности зарядка производиться не будет, поэтому проверьте правильность подключения «крокодильчиков» к клеммам батареи;
- зарядный ток необходимо выставить.
Если электролитная жидкость имеет слишком высокую или слишком низкую температуру, то приступать к зарядке нельзя. Дождитесь, когда жидкость станет комнатной температуры.
Постоянным током
Разновидность аккумуляторов определяет основные параметры зарядки:
- Если брать классическую АКБ, которая заполнена жидким электролитом, то величина заряда в этом случае не должна превышать показатель в 10% от ёмкости, указанной фирмой-производителем.

- Показатель в 10-30% характерен для AGM-аккумуляторов.
- Для АКБ с гелеобразным наполнителем эта цифра варьирует от 20 до 30%.
Постоянным напряжением
Для того, чтобы время зарядки кислотного аккумулятора не превышало допустимое, нельзя допускать полной потери емкости. Помните, что время зарядки напрямую зависит от количества остаточной ёмкости.
У аккумуляторной батареи, которая полностью разряжена, напряжение находится в пределах 12.7-13 В. Если включить мотор, то эти показатели увеличатся на 1.5 В. Стоит помнить, что оптимальная зарядка требует того, чтобы цифровые показатели напряжения не превышали 14,6 В. Если этот показатель превысить, то электронная жидкость закипит, произойдет перезарядка аккумулятора, а сам прибор придет в негодность.
Когда это нужно делать?
Необходимость в зарядке возникает тогда, когда:
- у генератора и аккумуляторной батареи выявлена неисправность цепи;
- при редком использовании автомобиля, либо при эксплуатации машины на небольшие расстояния;
- если запустить мотор на морозе.

Как влияет температура на процесс?
- Если температура составляет ниже — 15 градусов, то не рекомендуют производить зарядку аккумулятора, т.к. низкая температура может спровоцировать остановку работы механизма рекомбинации газов в герметичной ёмкости свинцового аккумулятора, при этом потеряется вода в электролите. Чтобы исправить недозаряд, необходимо подключать температурную компенсацию, равную – 3мВ /° С.
- При температуре более 40 градусов напряжение заряда уменьшается и может произойти перезарядка.
Обязательно ли снимать АКБ с машины, прежде чем подключить к устройству?
Многие автомобилисты стараются не снимать аккумулятор с машины для зарядки, мотивируя это тем, что после полной зарядки и установки АКБ на прежнее место возникают проблемы с электроникой. Такие опасения имеют под собой почву, поэтому если вы все же решили заряжать аккумулятор на машине, то постарайтесь придерживаться следующих правил:
- верхнюю поверхность следует хорошо очистить и включить выводы, предварительно сняв защитную крышку и выкрутив металлические болты;
- уровень электролита должен быть достаточным, при нехватке долейте дистиллированную воду, иначе вы не получите 100%-го заряда АКБ;
- подключать устройство в сеть следует только после того, как будет соблюдена полярность.

Какие есть особенности у зарядного устройства?
От правильной зарядки аккумулятора зависит очень многое. В исправной машине АКБ служит 2-3 года при пробеге 70-100 тыс км. Если батарея будет в заряженном состоянии, то ее срок службы значительно повысится. Рекомендуют заряжать аккумулятор в том случае, когда он станет разряжен наполовину, но при этом не стоит делать это слишком часто.
Схема доработки
Для того, чтобы АКБ не выходила из строя и прослужила долгое время, необходимо ее доработать. Для тех, кто в этом разбирается, можно найти в интернете различные схемы и пошаговые инструкции, как это сделать с наименьшими затратами.
Выбор выходного напряжения
Чтобы стабилизировать выходное напряжение, необходимо использовать TL431. Для делителя R2 напряжение всегда выдает 2.5 между R1 и R2. Это значит, что с такими показателями аккумулятор должен быть разряжен. Чтобы увеличить напряжение до 14.2 В при блоке питания 12 В необходимо изменить показатели R1 и R2: первый увеличить, а второй уменьшить.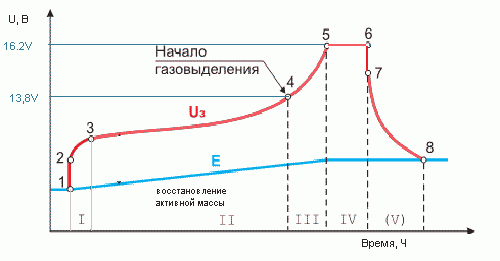 При этом блок питания выдаст 14.1. Этого достаточно для того, чтобы больше не менять данные делителя.
При этом блок питания выдаст 14.1. Этого достаточно для того, чтобы больше не менять данные делителя.
Схема зарядного устройства для свинцового аккумулятора с использованием TL431:
Добавление светодиода зеленого цвета и резистора r4 параллельно оптрону
Для стабилизации напряжения током в светодиоде оптрона управляет TL431.
При низком напряжении TL431 закрывается, останавливая ток в оптроне. Чтобы получать информацию о заряде аккумулятора необходимо поставить зеленый светодиод.
Ток оптрона при нормальном функционировании аккумулятора равен 0.5 мА – получаем слабое свечение зеленого светодиода. Для большей яркости необходимо подсоединить резистор R4 с номиналом в 220 Ом параллельно оптрону. Ток в зеленом диоде при этом увеличится до 5 мА.
Схема зарядного устройства свинцово кислотных аккумуляторов с добавлением светодиода зеленого цвета и резистора r4 параллельно оптрону:
Добавление петли гистерезиса ограничения тока
При большой перегрузке, такой, например, как короткое замыкание, необходимо сделать так, чтобы контроллер смог запустить БП.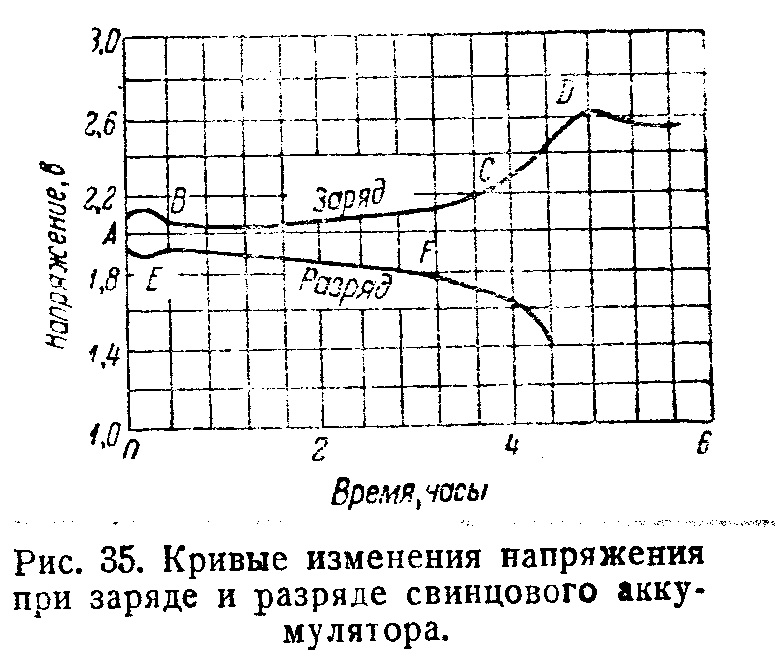 Для этого понадобится резистор мощности R5 и R6, красный светодиод и транзистор Т1. Переключатель включается параллельно с резисторами, при этом ток получает постоянное значение в 3.5 А. Недостаток такого соединение – сильное нагревание резисторов. Заменить одиночный резистор можно токовым зеркалом или операционным усилителем.
Для этого понадобится резистор мощности R5 и R6, красный светодиод и транзистор Т1. Переключатель включается параллельно с резисторами, при этом ток получает постоянное значение в 3.5 А. Недостаток такого соединение – сильное нагревание резисторов. Заменить одиночный резистор можно токовым зеркалом или операционным усилителем.
Схема зарядного устройства свинцово кислотных аккумуляторов с ограничением тока:
Кислотные аккумуляторы; чтобы больше не было отвратительно читать то что люди о них пишут / Хабр
Случайно узрел статью с комментариями к ней, и так злость во мне закипела по поводу безграмотности людей в области кислотных (свинцовых в простонародье) аккумуляторов, что не выдержал и решил написать «гикам» (чтобы быть гиком, как оказывается, мало купить дорогой телефон) краткую статью об аккумуляторах. С рассмотрением тех ошибок, которые мне постоянно мусолят глаза и вызывают праведное желание их исправить.
Начнем с названия.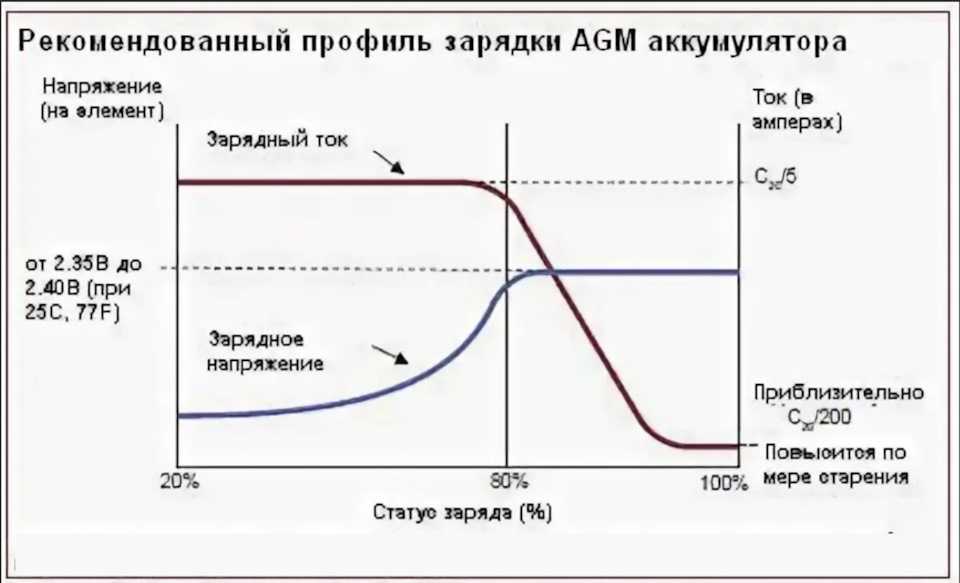 Я очень часто вижу что тремя буквами А-К-Б называют все что можно зарядить, абсолютно любой аккумулятор. Особенно тремя буквами люди любят называть аккумуляторы типа Li-ion. На самом-же деле АКБ аббревиатура от Аккумуляторная Кислотная Батарея. Под ними подразумевается лишь один тип аккумулятора — свинцовый кислотный. С современной точки зрения это название вызывает некоторый когнитивный диссонанс т.к. на данный момент значение слова «батарейка» т.е. гальванического элемента который зарядить нельзя перешло на слово «батарея». И получается как будто бы из-за слова «аккумуляторная» это аккумулятор который зарядить можно, а из-за слова «батарея» это как будто батарейка которую зарядить нельзя. В реальности-же батарея — просто цепь гальванических элементов и со словом «батарейка» имеет общий лишь корень.
Я очень часто вижу что тремя буквами А-К-Б называют все что можно зарядить, абсолютно любой аккумулятор. Особенно тремя буквами люди любят называть аккумуляторы типа Li-ion. На самом-же деле АКБ аббревиатура от Аккумуляторная Кислотная Батарея. Под ними подразумевается лишь один тип аккумулятора — свинцовый кислотный. С современной точки зрения это название вызывает некоторый когнитивный диссонанс т.к. на данный момент значение слова «батарейка» т.е. гальванического элемента который зарядить нельзя перешло на слово «батарея». И получается как будто бы из-за слова «аккумуляторная» это аккумулятор который зарядить можно, а из-за слова «батарея» это как будто батарейка которую зарядить нельзя. В реальности-же батарея — просто цепь гальванических элементов и со словом «батарейка» имеет общий лишь корень.
Далее перейдем к некоторым мифам, а именно главный миф — АКБ для автомобиля имеет некие существенные отличия от АКБ для ИБП. И вот нельзя их применять и там и там.
С химической точки зрения любые АКБ абсолютно одинаковы. Как-же они устроены? Очень кратко — если аккумулятор заряжен, то один электрод представляет собой свинцовую решетку с нанесенной на нее пастой из PbO2, второй -такую-же решетку с пастой губчатого свинца. Электролитом служит раствор серной кислоты. В процессе разряда PbO2 восстанавливается и взаимодействуя с серной кислотой образует PbSO4. Свинец на другом электроде окисляется и опять-же образует PbSO4. В конце разрядки мы имеем обе решетчатые пластины заполненные (более или менее) сульфатом свинца. При зарядке аккумулятора происходит электролиз и из сульфата свинца вновь образуется диоксид и металлический свинец. Конечно-же, тут нужно подчеркнуть, что электроды при этом не равны и путать их полярность не стоит т.к. еще на стадии производства в намазку электродов вводятся соответствующие добавки, улучшающие их эксплуатационные свойства. При этом добавки полезные для одного электрода вредны для другого. В очень старые времена, где-то в начале прошлого века, в условиях простых аккумуляторов, вероятно, была допустима переполюсовка аккумулятора по ошибке или с какими-то целями и он какое-то время после этого работал.
Как-же они устроены? Очень кратко — если аккумулятор заряжен, то один электрод представляет собой свинцовую решетку с нанесенной на нее пастой из PbO2, второй -такую-же решетку с пастой губчатого свинца. Электролитом служит раствор серной кислоты. В процессе разряда PbO2 восстанавливается и взаимодействуя с серной кислотой образует PbSO4. Свинец на другом электроде окисляется и опять-же образует PbSO4. В конце разрядки мы имеем обе решетчатые пластины заполненные (более или менее) сульфатом свинца. При зарядке аккумулятора происходит электролиз и из сульфата свинца вновь образуется диоксид и металлический свинец. Конечно-же, тут нужно подчеркнуть, что электроды при этом не равны и путать их полярность не стоит т.к. еще на стадии производства в намазку электродов вводятся соответствующие добавки, улучшающие их эксплуатационные свойства. При этом добавки полезные для одного электрода вредны для другого. В очень старые времена, где-то в начале прошлого века, в условиях простых аккумуляторов, вероятно, была допустима переполюсовка аккумулятора по ошибке или с какими-то целями и он какое-то время после этого работал. В том что она допустима сейчас я сомневаюсь.
В том что она допустима сейчас я сомневаюсь.
Таких ячеек в 12В аккумуляторе 6 шт, в 6В — 3 шт. и т.д. Многих вводит в заблуждение значение напряжения на аккумуляторах. Причем значений напряжения номинального, заряда, разряда. С одной стороны, аккумуляторы называются 12В (и 6В, 24В тоже есть, по-моему, даже 4В изредка встречаются) но на корпусе тех-же аккумуляторов для ИБП производитель указывает напряжение выше 13.5В.
Например:
Тут мы видим, что в форсированном режиме напряжение заряда может быть аж 15В.
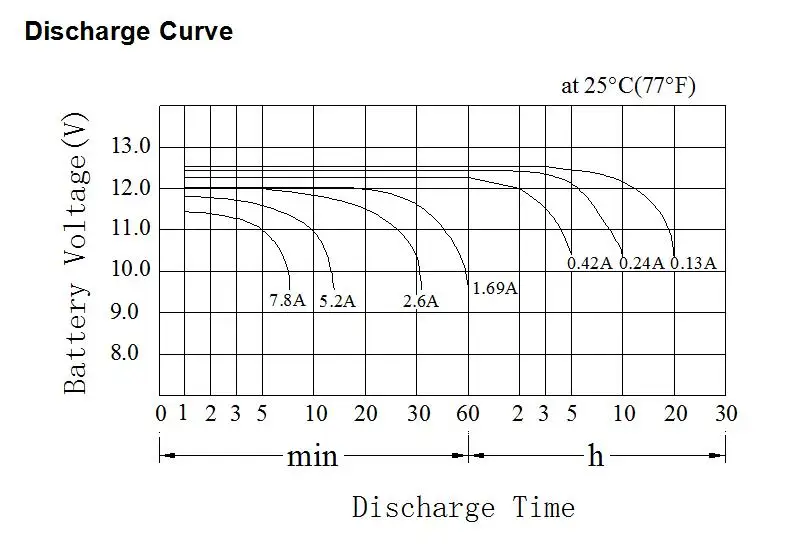
Все разъяснит кривая напряжения на АКБ:
Слева мы видим напряжение для аккумулятора из 12 ячеек (24В номинальных), 6 (12В номинальных) и, самое полезное, для одной ячейки. Там-же отмечены области нежелательных напряжений при разряде/ заряде. Из кривой можно сделать выводы:
1 Напряжение 12В, 24В и т.д. являются номинальными и показывают лишь число гальванических ячеек (путем деления на два) в батарее. Это просто название для удобства.
2 Напряжение при заряде могут достигать 2.5 В/ ячейку что для 12В аккумулятора соответствует 15В.
3 Напряжение заряженной батареи считается допустимым при значении 2.1-2.2 В/ячейку, что для 12В аккумулятора соответствует 12.6-13.2В.
Теоретически, батарею можно зарядить и до значений 2.4 В/ячейку или даже немного выше, однако, такая зарядка будет негативно сказываться как на состоянии электродов, так и на концентрации электролита. Однажды, перед сдачей в утиль, я легко зарядил 12В батарею до напряжения ок. 14.5В (уже не помню точное значение).
Итак, автор статьи с которой я начал, решил, что напряжение заряда автомобильной АКБ и АКБ от ИБП отличаются. Это неверно, у них одинаковый тип электродов и одинаковая концентрация серной кислоты в электролите (подобранная давным-давно экспериментальным путем, чтобы предоставлять максимальное напряжение и минимальном саморазряде). Однако, что-же происходит в батарее, почему ее нельзя заряжать при слишком высоком значении напряжения?
Почему в автомобильную АКБ нужно подливать воду, а в АКБ от ИБП не нужно? Эти вопросы позволяют нам плавно перейти в область напряжения разложения воды.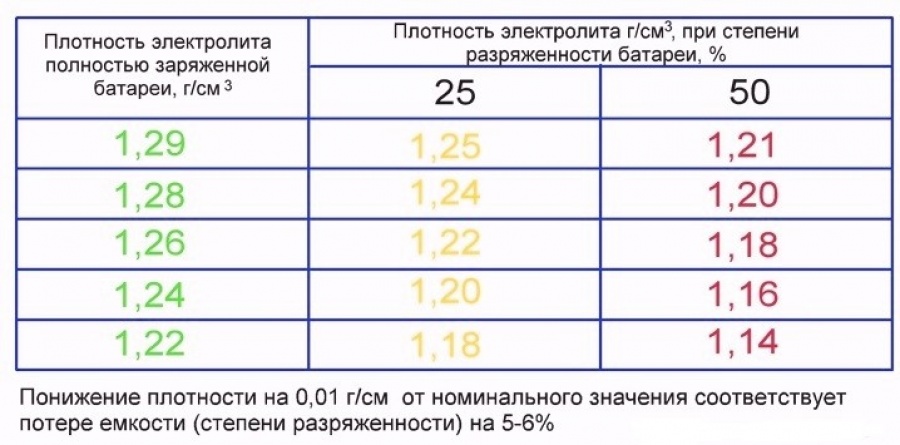 Как я написал выше, при зарядке аккумулятора происходит электролиз. Однако, не весь ток расходуется на превращение PbSO4 в PbO2 и Pb. Часть тока будет неизбежно расходоваться и на разложение воды, составляющей значительную часть электролита:
Как я написал выше, при зарядке аккумулятора происходит электролиз. Однако, не весь ток расходуется на превращение PbSO4 в PbO2 и Pb. Часть тока будет неизбежно расходоваться и на разложение воды, составляющей значительную часть электролита:
2H2O = 2H2 + O2
Теоретический расчет дает значение напряжения для этой реакции ок. 1.2В. Напоминаю, что напряжение на ячейке при заряде заведомо более 2В. К счастью, активно вода начинает разлагаться только выше 2В, а в промышленности для получения водорода и кислорода из нее процесс ведут и вовсе при 2.1-2.6В (при повышенной температуре). Как бы то ни было, тут мы приходим к выводу, что в конце процесса заряда АКБ будет неизбежно происходить процесс разложения воды в электролите на элементы. Образующиеся кислород и водород попросту улетучиваются из сферы реакции. Про них бытуют следующие мифы:
1. Водород крайне взрывоопасен! Перезарядишь аккумулятор и как минимум лишишься комнаты где тот был!
На самом деле, водорода в процессе электролиза выделяется ничтожно мало по сравнению с объемом комнаты.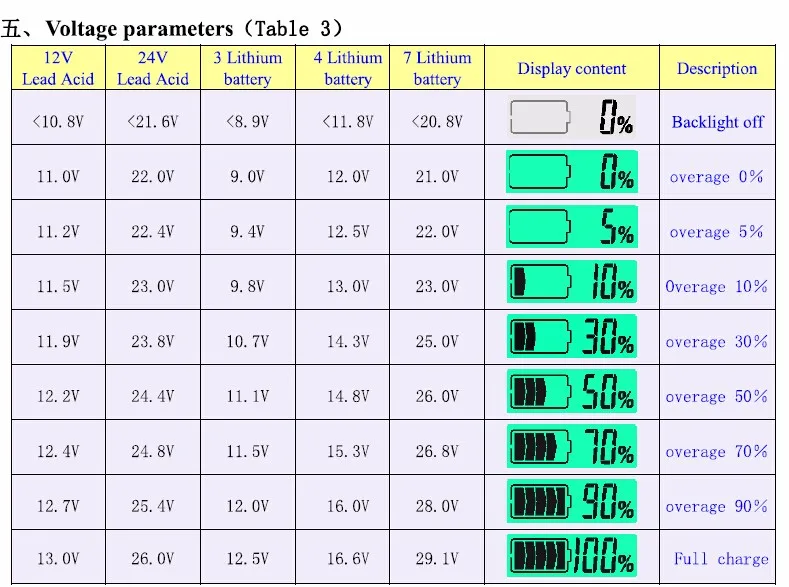 Водород взрывается при концентрации от 4% в воздухе. Если мы допустим, что электролиз ведется в комнате размером 3*3*3 метра или 27 метров куб., то нам понадобится наполнить помещение 27*0.04=1.1 метров куб. водорода. Для получения такого количества h3 нужно было бы полностью разложить ок. 49 моль воды или 884 грамма ее. Если кто-то наблюдал электролиз, то поймет насколько это много. Или попробуем перейти ко времени. При силе тока в стандартной зарядке для крупногабаритных АКБ в 6А, уравнение Фарадея дает время, необходимое для получения этого количества водорода, аж 437 часов или 18.2 дня. Чтобы наполнить комнату водородом до взрывоопасной концентрации нужно забыть про зарядку на 2 с половиной недели! Но даже если это случится, концентрация серной кислоты просто будет расти пока ее раствор не приобретет слишком высокое сопротивление для жалких 12В зарядки и сила тока не станет ничтожной. Да и водород попросту улетучится.
Водород взрывается при концентрации от 4% в воздухе. Если мы допустим, что электролиз ведется в комнате размером 3*3*3 метра или 27 метров куб., то нам понадобится наполнить помещение 27*0.04=1.1 метров куб. водорода. Для получения такого количества h3 нужно было бы полностью разложить ок. 49 моль воды или 884 грамма ее. Если кто-то наблюдал электролиз, то поймет насколько это много. Или попробуем перейти ко времени. При силе тока в стандартной зарядке для крупногабаритных АКБ в 6А, уравнение Фарадея дает время, необходимое для получения этого количества водорода, аж 437 часов или 18.2 дня. Чтобы наполнить комнату водородом до взрывоопасной концентрации нужно забыть про зарядку на 2 с половиной недели! Но даже если это случится, концентрация серной кислоты просто будет расти пока ее раствор не приобретет слишком высокое сопротивление для жалких 12В зарядки и сила тока не станет ничтожной. Да и водород попросту улетучится.
Очень редко случаются взрывы непосредственно в корпусах крупногабаритных АКБ из-за того, что выделяющийся водород по какой-то причине не может покинуть замкнутого пространства.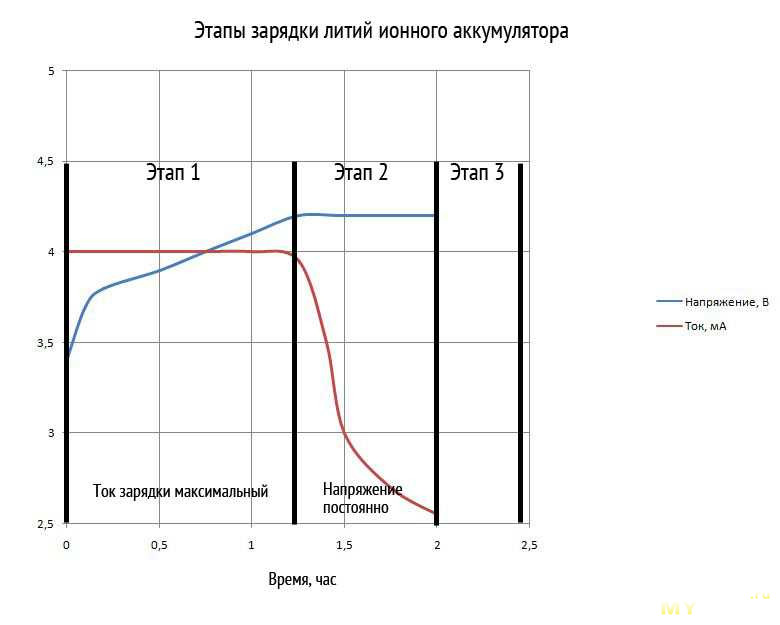 Но и в этом случае нечего страшного не бывает — чаще всего взрыва хватает только на небольшую деформацию верхней части корпуса, но не на разрыв свинцовых соединений. И АКБ еще может работать дальше даже после таких повреждений.
Но и в этом случае нечего страшного не бывает — чаще всего взрыва хватает только на небольшую деформацию верхней части корпуса, но не на разрыв свинцовых соединений. И АКБ еще может работать дальше даже после таких повреждений.
2. При электролизе может образоваться смертельно ядовитый и, не менее взрывоопасный чем водород, сероводород!
Не наш, периодически попадался миф в англоязычных постах. Теоретически конечно возможно подать такое большое напряжение и создать т.о. такую большую силу тока, что на катоде начнется процесс восстановления сульфат-иона. Напряжение для этого будет достаточным, а продукты восстановления не будут успевать диффундировать подальше от электрода и восстановление будет идти дальше. Но зарядка в пределах десятка-трех вольт и с ограничением силы тока в 6А на такое едва ли способна. Однажды, я наблюдал процесс восстановления сульфата до SO2, да, это возможно; однокурсницы по ошибке что-то сделали не то во время опыта. Но это большая редкость т.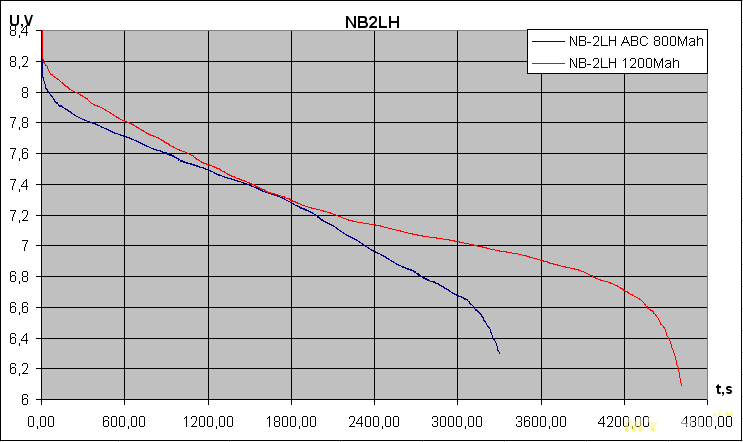 к. там концентрация серной кислоты была заметно выше той, что используется в АКБ, была иная конструкция электрода и иной его материал и, естественно, напряжения и сила тока были были непомерными. И SO2 не H2S.
к. там концентрация серной кислоты была заметно выше той, что используется в АКБ, была иная конструкция электрода и иной его материал и, естественно, напряжения и сила тока были были непомерными. И SO2 не H2S.
3. При электролизе мышьяк и сурьма из материала решеток будут восстанавливаться до ядовитых арсина и стибина!
Действительно, решетки содержат относительно много сурьмы, мышьяка в современных решетках, вероятно, нет вообще. При работе АКБ та решетка на которой происходит восстановление, т.е. катод, разрушению не может подвергаться. Выделяйся даже каким-то образом стибин, он бы тут-же взаимодействовал с PbSO4, восстанавливая его до металла.
Однако, некоторая практическая неприятность тут есть. Газообразные водород и кислород могут увлекать за собой капельки электролита, создавая аэрозоль серной кислоты. Аэрозоль серной кислоты, даже концентрированной, для человека не опасен и просто вызывает кашель. Однако, серная кислота — кошмар для тканей и бумаги.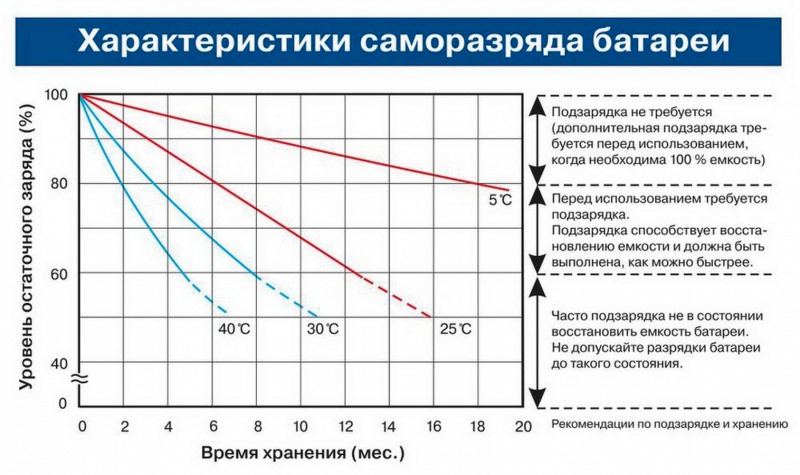 Стоит даже небольшому количеству серной кислоты попасть на одежду и там обязательно появятся дырки или ткань разорвется по этому месту. Через недели, если кислоты много, через месяц, но одежда истлеет.
Стоит даже небольшому количеству серной кислоты попасть на одежду и там обязательно появятся дырки или ткань разорвется по этому месту. Через недели, если кислоты много, через месяц, но одежда истлеет.
Так что газовыделения опасаться не стоит с бытовой точки зрения или стоит, но нужно ориентироваться именно на аэрозоль серной кислоты.
Итак, вода начала разлагаться на водород кислород, ее в электролите становится все меньше, что-же дальше? Если это АКБ в котором электролит просто налит в виде слоя жидкости, то начнется повышение саморазряда из-за повышения концентрации серной кислоты. Занятно, что это будет сопровождаться небольшим повышением напряжения (концентрация кислоты растет) на ячейке. Именно поэтому автовладельцы должны постоянно контролировать концентрацию серной кислоты в своих АКБ (при помощи ареометра) и доливать туда воду. Процедура доливания воды — необходимая часть процесса обслуживания любой АКБ. Кроме одного их типа, и мы сейчас об этом поговорим.
Иметь аккумулятор в котором болтается слой едкой, по отношению к металлам, жидкости конечно-же неудобно, а потому попытки избавиться непосредственно от жидкости предпринимались давно, начались чуть ли не в первой половине 20-го века. К слову сказать, не то чтобы слой серной кислоты прямо плескался вокруг электродов. В реальности она неплохо распределена между электродами и окружающими их сепараторами даже в дешевых моделях. Итак, первым вариантом было использование стекловолокна. Достаточно просто окружить электроды стекловолокном которое пропитано серной кислотой и большинство проблем решится. Этот тип АКБ носит название AGM (absorbent glass mat) и таких АКБ для ИБП подавляющее большинство. Хотя такие АКБ малого форм-фактора и зачастую позиционируются как те, которые можно эксплуатировать в любом положении, с этим нельзя вполне согласиться. Вскрытие крышки стандартного дешевого AGM аккумулятора показывает, что никаких особых крышек там нет, а следовательно, электролит от вытекания удерживают лишь капиллярные силы. Я почти уверен, что если погонять AGM аккумулятор перевернутым вверх дном, то уже после одной зарядки из него польется серная кислота под давление газов.
К слову сказать, не то чтобы слой серной кислоты прямо плескался вокруг электродов. В реальности она неплохо распределена между электродами и окружающими их сепараторами даже в дешевых моделях. Итак, первым вариантом было использование стекловолокна. Достаточно просто окружить электроды стекловолокном которое пропитано серной кислотой и большинство проблем решится. Этот тип АКБ носит название AGM (absorbent glass mat) и таких АКБ для ИБП подавляющее большинство. Хотя такие АКБ малого форм-фактора и зачастую позиционируются как те, которые можно эксплуатировать в любом положении, с этим нельзя вполне согласиться. Вскрытие крышки стандартного дешевого AGM аккумулятора показывает, что никаких особых крышек там нет, а следовательно, электролит от вытекания удерживают лишь капиллярные силы. Я почти уверен, что если погонять AGM аккумулятор перевернутым вверх дном, то уже после одной зарядки из него польется серная кислота под давление газов.
Второй распространенный тип интереснее, это т._641x420.jpg) н. гелевые АКБ. А получаются они благодаря следующему. Если подкислять растворимые силикаты, то будет происходить выделение кремневой кислоты:
н. гелевые АКБ. А получаются они благодаря следующему. Если подкислять растворимые силикаты, то будет происходить выделение кремневой кислоты:
Na2SiO3 + H2SO4 = Na2SO4 + SiO2 + H2O
Если исходный раствор силиката не отличается качеством, то кремневая кислота будет выделяться в виде стекловидной массы, но если он достаточно чист, то кремневая кислота осадится в виде красивого куска однородного полупрозрачного геля. На этом и основан способ получения гелевых АКБ — простое добавление силикатов к электролиту вызывает его затвердение в гелеобразную массу. Соответственно, вытекать оттуда уже нечему и АКБ действительно можно эксплуатировать в любом положении. Сам по себе процесс образования геля не повышает емкости АКБ и не улучшает его качеств, однако, производители его используют при производстве наиболее качественных моделей, а потому эти АКБ отличаются высоким качеством и большей емкостью. Занятно, что в обоих случаях носителем электролита является SiO2 в той или иной форме.
Занятно, что в обоих случаях носителем электролита является SiO2 в той или иной форме.
Оба типа АКБ объединяются в славный тип VRLA — valve-regulated lead-acid battery который и применяется в ИБП. Формально они считаются необслуживаемыми и терпящими эксплуатацию в любом положении, но это не совсем так. Более того, многие уже встречались с эффектом, когда буквально несколько мл воды возвращают к жизни, казалось бы, дохлую АКБ от ИБП. Так получается, потому что и эти аккумуляторы не капли не застрахованы от электролиза воды в электролите, а следовательно, и пересыхания. Все происходит точно так-же, как в крупногабаритных АКБ. А вот самые дорогие и крутые необслуживаемые АКБ содержат катализатор для рекомбинации выделяющихся газов обратно в воду и вот уже у них корпус действительно выполнен абсолютно герметичным. Обращаю внимание, что по-настоящему герметичным и необслуживаемым может быть и аккумулятор типа AGM и GEL, но они-же могут ими и не быть и не содержать катализатора рекомбинации кислорода и водорода. Тогда, несмотря на казалось бы продвинутую конструкцию, пользователю придется либо чаще покупать новые аккумуляторы, либо доливать воду при помощи шприца.
Тогда, несмотря на казалось бы продвинутую конструкцию, пользователю придется либо чаще покупать новые аккумуляторы, либо доливать воду при помощи шприца.
Хотелось бы добавить несколько слов о режимах разряда. Производители АКБ указывают какой ток максимально допустим для той или иной модели, но нужно понимать, что аккумулятор — просто смесь химических веществ и ЭДС генерируется исключительно химическим путем. Это не конденсатор который, по электрогидравлической аналогии, можно сравнить с неким механическим сосудом (с гибкой мембраной). Хотя АКБ могут выдавать очень большие значения силы тока, в реальности они лучше всего эксплуатируются как раз при небольших токах, что в разряде, что в заряде. Поэтому ИБП, рассчитанные на заряды небольших АКБ, при работе с крупногабаритными будут заряжать их в наиболее щадящем режиме. Впрочем, в течении далеко не одних суток. Интересно обратить внимание на то, что чем выше мощность ИБП, тем больше аккумуляторов последовательно предпочитает собирать производитель. Тут все логично — большие токи разряда маленькие АКБ выдерживают очень плохо.
Тут все логично — большие токи разряда маленькие АКБ выдерживают очень плохо.
Подводя итоги:
1. Малогабаритные и крупногабаритные АКБ идентичны по устройству.
2. Для подавляющего большинства АКБ любого размера доливание воды является необходимой частью текущего обслуживания.
3. Лишь немногие из дорогих моделей АКБ содержат механизм рекомбинации газов и могут быть названы действительно необслуживаемыми.
4. Сам по себе водород, который выделяется при заряде (а это равно постоянной работе в ИБП) АКБ, не является существенной угрозой или проблемой.
5. Нужно очень внимательно работать с АКБ, тщательно избегая пролива даже малейших капель электролита, или лишитесь одежды.
6. Разряд и заряд малыми токами являются наиболее предпочтительными режимами эксплуатации АКБ.
Графики напряжения свинцово-кислотных аккумуляторов (6 В, 12 В и 24 В)
Ниже приведены графики напряжения свинцово-кислотных аккумуляторов, показывающие состояние заряда в зависимости от напряжения для аккумуляторов 6 В, 12 В и 24 В, а также для свинцово-кислотных элементов 2 В.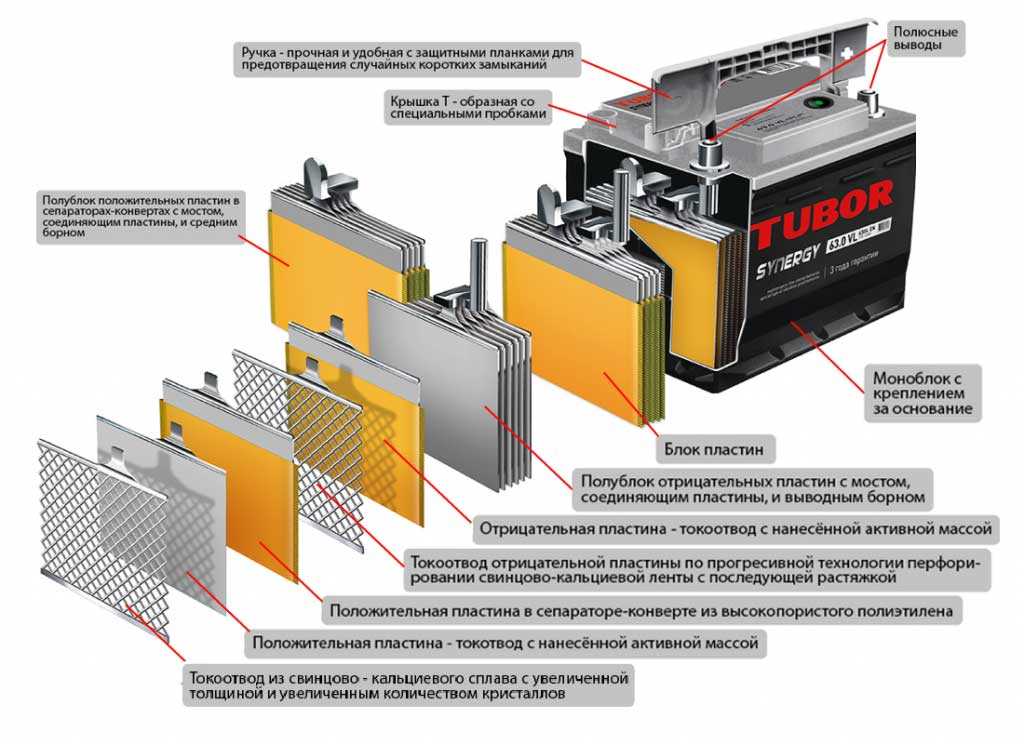
Кривые напряжения свинцово-кислотного аккумулятора сильно различаются в зависимости от таких переменных, как температура, скорость разряда и тип аккумулятора (например, герметичный, залитый). График зависимости напряжения от емкости аккумулятора в руководстве по эксплуатации аккумулятора всегда должен иметь приоритет над общими усредненными значениями, перечисленными ниже.
Примечание: Оценка состояния заряда на основе напряжения холостого хода является точной только тогда, когда батареи находятся при комнатной температуре и находятся в состоянии покоя, т.е. отключены от всех нагрузок и зарядных устройств, в течение нескольких часов.
6V Диаграммы напряжения кислотной батареи.V
 98V
98VТаблица для печати
6V Flooded Lead Acid Batteries
| Voltage | Capacity |
|---|---|
| 6.32V | 100% |
| 6.26V | 90% |
| 6.20V | 80% |
| 6.15V | 70% |
| 6.09V | 60% |
| 6.03V | 50% |
| 5,98V | 30% |
| 5.88V | 20% |
| 5.82V | 10% |
| 5.79V | 0% |
Printable Chart
Notes
6V lead acid батареи используются в некоторых устройствах постоянного тока, таких как фонари, насосы и электрические велосипеды. Вы также можете соединить два последовательно, чтобы создать аккумуляторную батарею на 12 В. Они изготавливаются путем последовательного соединения трех свинцово-кислотных аккумуляторов на 2 В.
Вы также можете соединить два последовательно, чтобы создать аккумуляторную батарею на 12 В. Они изготавливаются путем последовательного соединения трех свинцово-кислотных аккумуляторов на 2 В.
6 В герметичные свинцово-кислотные аккумуляторы полностью заряжаются при напряжении около 6,44 В и полностью разряжаются при напряжении около 6,11 В (при максимальной глубине разряда 50 %).
6 В залитые свинцово-кислотные аккумуляторы полностью заряжены при напряжении около 6,32 В и полностью разряжены при напряжении около 6,03 В (при максимальной глубине разряда 50%).
12 В свинцовой кислотной батареи. %
 70V
70VPrintable Chart
12V Flooded Lead Acid Batteries
| Voltage | Capacity | |
|---|---|---|
| 12.64V | 100% | |
| 12.53V | 90% | |
| 12.41V | 80% | |
| 12.29V | 70 | |
| .0016 | 11,76 В | 20% |
| 11,63 В | 10% | |
| 11,59 В | 0% | 0% 91919 В | 0% 9191 |
919191919191919191919191919111111111111111111111119. и другие электрические системы 12В. Они широко доступны и имеют низкую начальную стоимость. Многие автомобильные и морские аккумуляторы представляют собой свинцово-кислотные аккумуляторы на 12 В. Они изготавливаются путем последовательного соединения шести свинцово-кислотных аккумуляторов на 2 В.
Насколько я могу судить, свинцово-кислотные аккумуляторы по-прежнему являются самым популярным типом аккумуляторов для самодельных солнечных электростанций. Литий-железо-фосфатные (LiFePO4) батареи в последние годы стали намного более популярными, во многом благодаря их резкому падению цен, которое мы наблюдали за последнее десятилетие.
12 В герметичные свинцово-кислотные аккумуляторы полностью заряжаются при напряжении около 12,89 В и полностью разряжаются при напряжении около 12,23 В (при максимальной глубине разряда 50%).
12 В залитые свинцово-кислотные аккумуляторы полностью заряжены при напряжении около 12,64 В и полностью разряжены при напряжении около 12,07 В (при максимальной глубине разряда 50%).
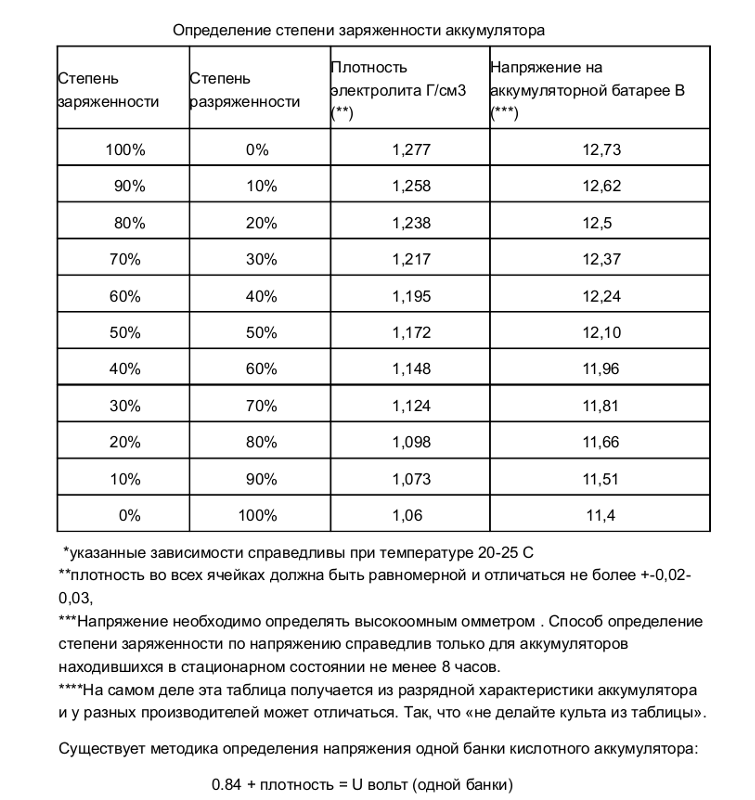
Таблицы напряжения свинцово-кислотных аккумуляторов 24 В
Герметичные свинцово-кислотные аккумуляторы 24 В (AGM и гелевые)
| Напряжение | Capacity |
|---|---|
25. 77V 77V | 100% |
| 25.56V | 90% |
| 25.31V | 80% |
| 25.02V | 70% |
| 24.81 V | 60% |
| 24.45V | 50% |
| 24.21V | 40% |
| 23.91V | 30% |
| 23.61V | 20% |
| 23.40V | 10% |
| 23.25V | 0% |
Printable Chart
24V Flooded Lead Acid Batteries
| Voltage | Capacity |
|---|---|
| 25.29V | 100% |
| 25.05V | 90% |
| 24.81V | 80% |
| 24.58V | 70% |
| 24.36V | 60% |
| 24.14V | 50% |
23. 94V 94V | 40% |
| 23.74V | 30% |
| 23.51V | 20% |
| 23.27V | 10 % |
| 23,18 В | 0 % |
Таблица для печати
Примечания
24 В для солнечных батарей. Работа с более высоким напряжением помогает поддерживать низкую силу тока, экономя деньги на проводке и оборудовании. Они изготавливаются путем последовательного соединения двенадцати свинцово-кислотных элементов по 2 В или двух свинцово-кислотных аккумуляторов по 12 В.
24 В герметичные свинцово-кислотные аккумуляторы полностью заряжаются при напряжении около 25,77 В и полностью разряжаются при напряжении около 24,45 В (при максимальной глубине разряда 50 %).
24 В залитые свинцово-кислотные аккумуляторы полностью заряжены при напряжении около 25,29 В и полностью разряжены при напряжении около 24,14 В (при максимальной глубине разряда 50%).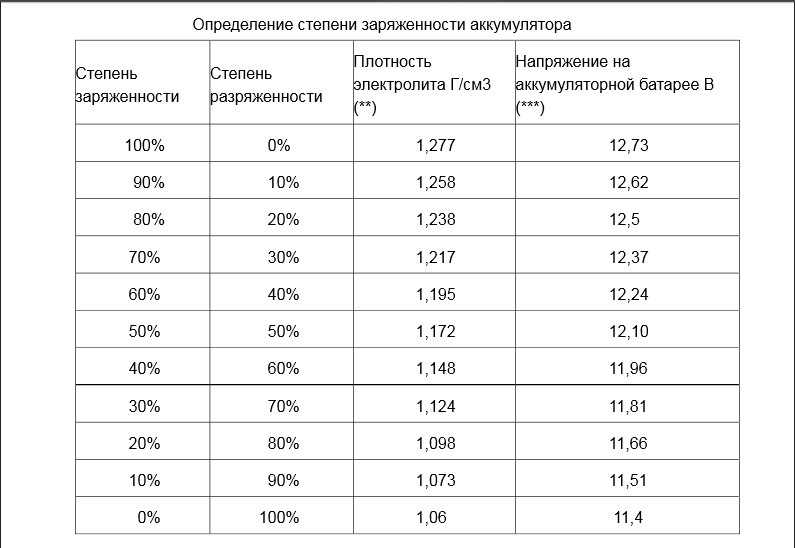
Таблицы напряжения свинцово-кислотного элемента 2 В
Герметичные свинцово-кислотные элементы 2 В (AGM и гель)
| Напряжение | Capacity |
|---|---|
| 2.15V | 100% |
| 2.13V | 90% |
| 2.11V | 80% |
| 2.09V | 70% |
| 2.07 V | 60% |
| 2.04V | 50% |
| 2.02V | 40% |
| 1.99V | 30% |
| 1.97V | 20% |
| 1.95V | 10% |
| 1.94V | 0% |
Printable Chart
2V Flooded Lead Acid Cells
| Voltage | Capacity |
|---|---|
| 2.11V | 100% |
| 2,09 В | 90% |
| 2,07V | 80% |
| 2,05V | |
| 2,05V | |
| 2.01V | 50% |
| 1.99V | 40% |
| 1.98V | 30% |
| 1.96V | 20% |
| 1.94V | 10% |
| 1,93 В | 0% |
Таблица для печати
Примечания
Номинальное напряжение отдельных свинцово-кислотных элементов составляет 2 вольта (иногда указывается как 2,1 вольта). Вы можете купить свинцово-кислотные элементы на 2 В и соединить их последовательно-параллельно, чтобы создать банк батарей с желаемым напряжением и емкостью.
2 В герметичные свинцово-кислотные элементы полностью заряжаются при напряжении около 2,15 В и полностью разряжаются при напряжении около 2,04 В (при максимальной глубине разряда 50%).
2 В залитые свинцово-кислотные элементы полностью заряжаются при напряжении около 2,11 В и полностью разряжаются при напряжении около 2,01 В (при максимальной глубине разряда 50%).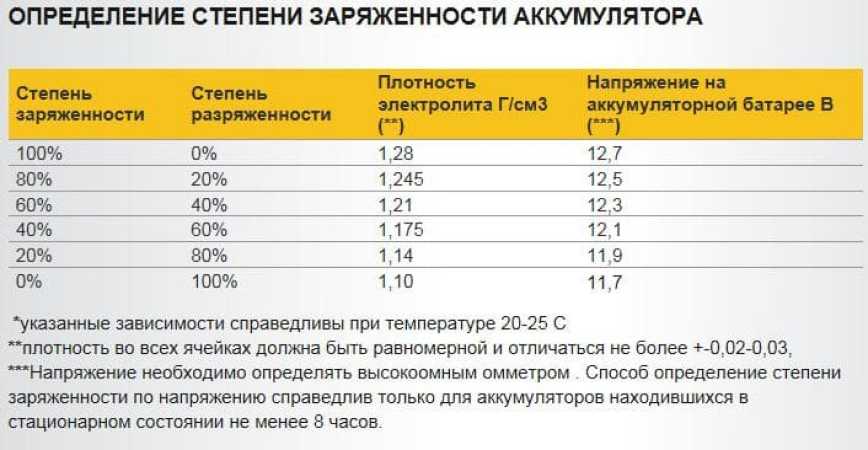
3 способа проверить емкость свинцово-кислотного аккумулятора
1. Измерить напряжение холостого хода с помощью мультиметра
Плюсы: Точность
Минусы: Необходимо отключить все нагрузки и зарядные устройства и дать аккумулятору отдохнуть в течение нескольких часов
Чтобы правильно оценить емкость аккумулятора на основе напряжения холостого хода, сначала отключите все от аккумулятора и дайте ему отдохнуть при комнатной температуре в течение нескольких часов. (Университет аккумуляторов рекомендует не менее 4 часов.)
Затем просто измерьте мультиметром напряжение на клеммах аккумулятора и сравните полученное значение с диаграммой состояния заряда в руководстве по эксплуатации аккумулятора. Если в вашем руководстве по аккумулятору нет таблицы, используйте соответствующую таблицу, указанную выше.
Например, недавно я хотел проверить оставшуюся емкость принадлежащей мне герметичной свинцово-кислотной батареи 12 В 33 Ач.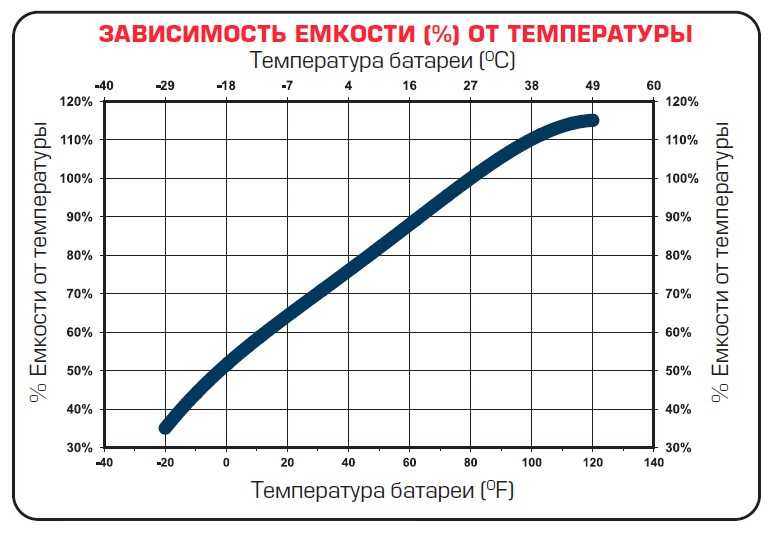 Батарея уже находилась в покое и при комнатной температуре — последние пару недель она лежала отключенной в моем подвале.
Батарея уже находилась в покое и при комнатной температуре — последние пару недель она лежала отключенной в моем подвале.
Итак, я схватил свой мультиметр, приготовил его для измерения напряжения постоянного тока и приложил щупы к клеммам аккумулятора. У меня получилось напряжение холостого хода 12,63 вольта.
Я не смог найти руководство по эксплуатации своего аккумулятора, поэтому я сослался на приведенную выше таблицу напряжения 12-вольтового свинцово-кислотного аккумулятора, чтобы оценить его емкость. Основываясь на этой диаграмме, я оценил, что осталось около 80% емкости.
2. Проверка удельного веса с помощью ареометра или рефрактометра
Плюсы: Точно
Минусы: Подходит только для залитых свинцово-кислотных аккумуляторов
Вы можете использовать ареометр или рефрактометр для измерения так называемого удельного веса свинцово-кислотный аккумулятор. Измерение удельного веса — еще один способ оценить состояние заряда.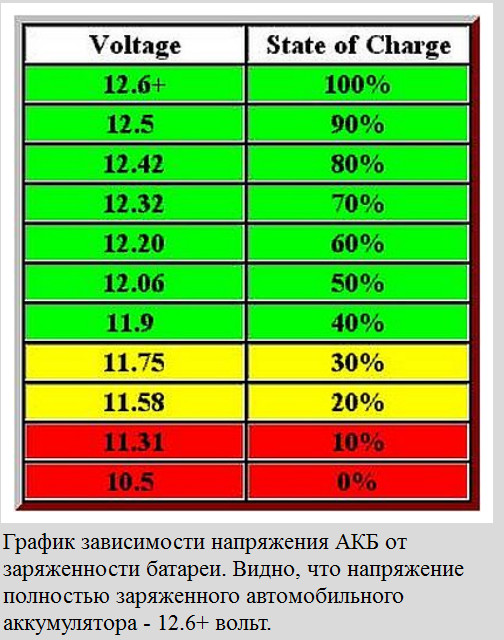
Поскольку этот метод требует открытия батареи для доступа к раствору электролита внутри, он работает только с залитыми батареями.
Я когда-либо использовал только герметичные свинцово-кислотные батареи, поэтому, к сожалению, не могу объяснить вам, как это сделать. См. шаги, перечисленные в руководстве по эксплуатации вашего аккумулятора или в руководстве по эксплуатации вашего ареометра или рефрактометра.
3. Используйте контроллер заряда от солнечной батареи
Плюсы: Удобно
Минусы: Неточно
Если вы используете свинцово-кислотную батарею в системе солнечной энергии, контроллер заряда, вероятно, измеряет напряжение батареи для вас.
Возможно, вы думаете, что можете просто использовать эти показания, чтобы получить точную оценку емкости аккумулятора. К сожалению, использование напряжения батареи для оценки емкости, когда батарея подключена к зарядным устройствам и нагрузкам, очень неточна.
Напряжение батареи сильно зависит от таких факторов, как температура и скорость разрядки. Кроме того, показания напряжения батареи, выдаваемые некоторыми контроллерами заряда, могут быть неточными. Некоторые контроллеры заряда отображают только один десятичный разряд, а другие имеют большие пределы погрешности. Например, один дешевый ШИМ-контроллер заряда, который я тестировал, заявлял, что погрешность напряжения батареи составляет ± 0,2 вольта.
Кроме того, показания напряжения батареи, выдаваемые некоторыми контроллерами заряда, могут быть неточными. Некоторые контроллеры заряда отображают только один десятичный разряд, а другие имеют большие пределы погрешности. Например, один дешевый ШИМ-контроллер заряда, который я тестировал, заявлял, что погрешность напряжения батареи составляет ± 0,2 вольта.
Тем не менее, я знаю, что большинство энтузиастов, занимающихся самодельной солнечной энергетикой, будут использовать это значение чаще всего, если не исключительно. Довольно хлопотно отсоединить все от аккумулятора и дать ему отдохнуть только для более точного измерения состояния его заряда.
Если это вы, просто имейте в виду, насколько неточным может быть этот номер. Не думайте, что по нему можно узнать точное состояние заряда аккумулятора. Просто используйте его, чтобы получить общее представление о том, близка ли ваша батарея к полной зарядке или разрядке.
Часто задаваемые вопросы о напряжении свинцово-кислотной батареи
Примечание: Повторим еще раз: рекомендуемые напряжения и диаграммы состояния заряда в руководстве по эксплуатации вашей батареи должны иметь приоритет над общими, перечисленными ниже.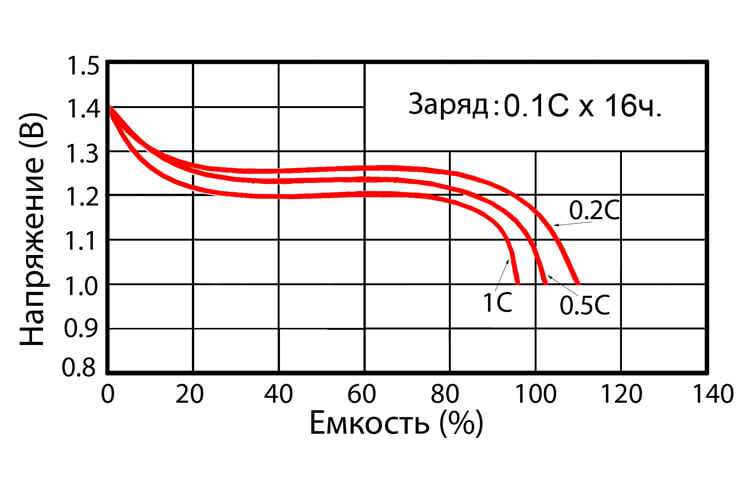
Каково напряжение полностью заряженной свинцово-кислотной батареи 12 В?
12-вольтовая герметичная свинцово-кислотная батарея будет иметь напряжение холостого хода около 12,9 В при полной зарядке.
Залитая свинцово-кислотная батарея 12 В будет иметь напряжение холостого хода около 12,6 В при полной зарядке.
Чтобы точно оценить емкость аккумулятора по напряжению, необходимо сначала отключить все нагрузки и зарядные устройства от аккумулятора и оставить его при комнатной температуре на несколько часов.
Каково минимальное напряжение 12-вольтовой свинцово-кислотной батареи?
Минимальное напряжение холостого хода 12-вольтовой герметичной свинцово-кислотной батареи составляет около 12,2 В при максимальной глубине разряда 50 %.
Минимальное напряжение холостого хода 12В залитой свинцово-кислотной батареи составляет около 12,1 В при максимальной глубине разряда 50%.
Насколько можно разрядить свинцово-кислотный аккумулятор?
Многие свинцово-кислотные аккумуляторы можно разряжать только до 50 %. Разрядка их больше может привести к необратимому повреждению. Вы никогда не должны полностью разряжать свинцово-кислотный аккумулятор до 100% глубины разряда. Это может значительно сократить срок его службы.
Вот график, показывающий взаимосвязь между глубиной разряда и жизненным циклом свинцово-кислотных аккумуляторов без глубокого цикла:
Источник: PVEducation
Как видите, постоянная разрядка свинцово-кислотного аккумулятора до 100 % может значительно сократить срок его службы. .
Каково остаточное напряжение 12-вольтовой свинцово-кислотной батареи?
Плавающее напряжение герметичной свинцово-кислотной батареи 12 В обычно составляет 13,6 В ± 0,2 В.
Плавающее напряжение 12-вольтовой свинцово-кислотной батареи с заливкой обычно составляет 13,5 вольт.
Как всегда, ориентируйтесь на рекомендованное напряжение подзаряда, указанное в руководстве к вашей батарее.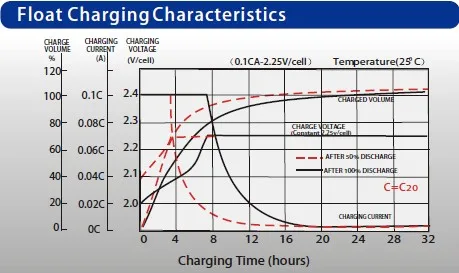 Некоторые бренды называют поплавок «ожиданием». Иногда плавающее напряжение даже указывается на этикетке аккумулятора.
Некоторые бренды называют поплавок «ожиданием». Иногда плавающее напряжение даже указывается на этикетке аккумулятора.
Рекомендуемое плавающее напряжение может быть указано на этикетке вашей батареи как «напряжение в режиме ожидания» или «использование в режиме ожидания».
Как я получил числа в этих таблицах
Чтобы получить числа в приведенных выше таблицах напряжений, я просмотрел спецификации для 7 популярных марок свинцово-кислотных аккумуляторов. Я нашел диаграммы состояния заряда в каждом и усреднил их вместе для получения окончательных значений.
Вот таблицы данных, которые я использовал для герметичных свинцово-кислотных значений (2 AGM, 2 геля), вместе с номером страницы, где я нашел диаграмму напряжения:
- Power-Sonic (стр. 10)
- Fullriver (стр. 10) 23)
- Universal Battery (стр. 2)
- Renogy (стр. 4)
Вот те, которые я использовал для залитых значений:
- Crown (стр. 6)
- Trojan Battery (стр.
 1)
1) - OutBack Power (стр. 8)
Создание этих карт было далеко от точной науки. Только в нескольких таблицах данных напряжения холостого хода указаны по емкости в табличном формате с точными числами. Часто они включали график, из которого мне приходилось делать выводы. Более того, на графиках часто были широкие полосы, а не тонкие линии, как бы показывающие предел погрешности или диапазон возможных значений — то, что я пришел к выводу, что бренды хеджируют от предоставления точного числа.
Другие бренды предоставили точные цифры, но только для значений емкости 0%, 25%, 50%, 75% и 100%. Из них мне пришлось создать линейные функции для оценки значений между ними.
Сначала я рассчитал все значения для свинцово-кислотных аккумуляторов на 2 В, а затем умножил эти значения на соответствующее количество последовательно соединенных элементов, чтобы получить значения для аккумуляторов на 6 В, 12 В и 24 В. Наконец, я округлил все значения до двух знаков после запятой.
аккумуляторов — Каким должно быть напряжение полностью заряженного свинцово-кислотного аккумулятора?
спросил
Изменено
1 год, 5 месяцев назад
Просмотрено
92к раз
\$\начало группы\$
У меня нет подходящего зарядного устройства для свинцово-кислотных аккумуляторов… Но у меня есть небольшой аккумулятор Yuasa емкостью 7 Ач. Я использую настенную бородавку 13 вольт 1,5 А для зарядки. И у меня есть вольтметр, чтобы проверить напряжение.
При каком напряжении следует снимать аккумулятор с зарядного устройства?
- аккумуляторы
- зарядные аккумуляторы
- свинцово-кислотные
\$\конечная группа\$
\$\начало группы\$
См.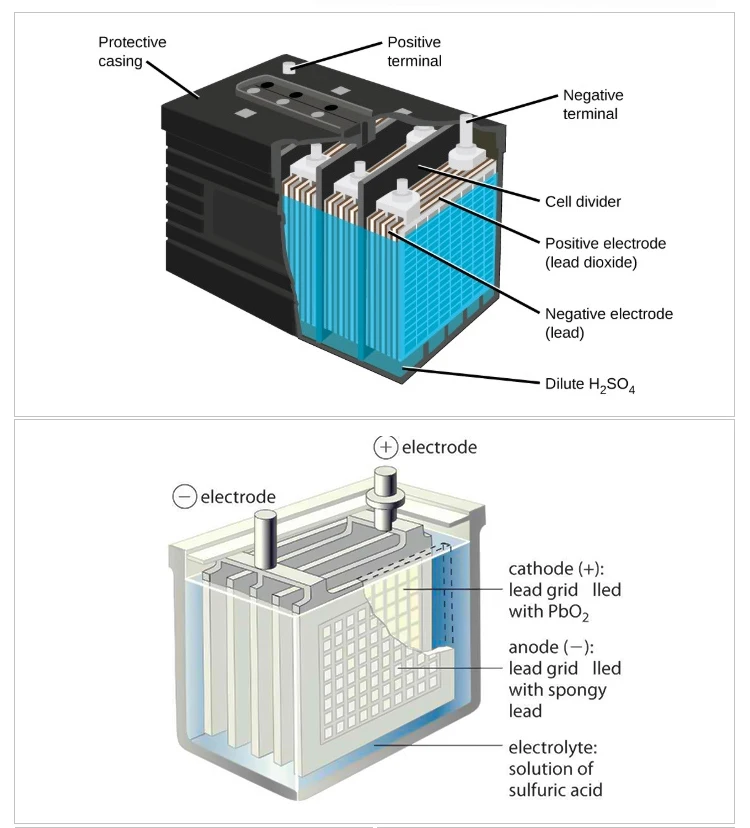 мой ответ по обмену стеками на «Факторы конструкции зарядного устройства для свинцово-кислотных аккумуляторов», который касается, и перейдите по ссылке на сайт Университета аккумуляторов, который расскажет вам гораздо больше, чем вы знали о свинцово-кислотных (и других) батареях. .
мой ответ по обмену стеками на «Факторы конструкции зарядного устройства для свинцово-кислотных аккумуляторов», который касается, и перейдите по ссылке на сайт Университета аккумуляторов, который расскажет вам гораздо больше, чем вы знали о свинцово-кислотных (и других) батареях. .
Из приведенного выше ответа обратите внимание на цитаты с вышеуказанного веб-сайта. Особенно в этом контексте
Правильная настройка напряжения заряда имеет решающее значение, и
находится в диапазоне от 2,30 до 2,45 В на элемент .
Установка порога напряжения является компромиссом, и эксперты по аккумуляторным батареям называют это «танцами на острие иглы».
С одной стороны, батарея хочет быть полностью заряжена, чтобы получить максимальную емкость и избежать сульфатации на отрицательной пластине; с другой стороны, состояние перенасыщения вызывает коррозию сетки на положительной пластине и вызывает выделение газов.Чтобы затруднить «танцы на острие иглы», напряжение батареи меняется в зависимости от температуры.
 Более теплая среда требует немного более низких порогов напряжения, а холодная окружающая среда предпочитает более высокий уровень.
Более теплая среда требует немного более низких порогов напряжения, а холодная окружающая среда предпочитает более высокий уровень.
2,30 x 6 = 13,8 В
2,45 x 6 = 14,7 В
13,8 В — номинальное напряжение, при котором работают многие автомобильные системы.
14,7 В выше, чем вы обычно встречаете, но около 14,4 В обычно используется для зарядки в режиме «долива», который используется для выравнивания заряда в последовательно соединенных ячейках. Посетите сайт Battery University, чтобы получить НАМНОГО больше информации.
Если вы заряжаете только до 12,6 В, как рекомендовали несколько человек, ваша батарея никогда не будет работать на полную мощность, и ее срок службы сократится.
См. также Безопасная рабочая зона для различных типов аккумуляторов?
А также Можно ли зарядить 12В герметичный свинцово-кислотный аккумулятор от старой настенной бородавки (не предназначенной для зарядки)?
А также Зарядка свинцово-кислотных аккумуляторов?
\$\конечная группа\$
3
\$\начало группы\$
Аккумуляторы глубокого цикла заряжаются в 3 этапа: общий заряд, долив и плавающий заряд. Во время объемного заряда очень важна плотность тока (А/см² или А/дм²). Если ток меньше, чем необходимо для поверхности электродов, появится кристаллическая структура. Губчатый материал обратим, но кристаллический материал необратим, и это очень важно и для PbSO₄.
Во время объемного заряда очень важна плотность тока (А/см² или А/дм²). Если ток меньше, чем необходимо для поверхности электродов, появится кристаллическая структура. Губчатый материал обратим, но кристаллический материал необратим, и это очень важно и для PbSO₄.
После заряда батареи до 80% ток уменьшается и при подзаряде составляет менее 1 Ампера.
Лучше всего использовать умное зарядное устройство. То, как батарея используется и обслуживается, может увеличить срок службы батареи с 6 месяцев до 7 лет. Никогда не оставляйте разряженную батарею незаряженной; разрядка аккумулятора на 50 % перед зарядкой может продлить срок службы аккумулятора в 2–3 раза.
\$\конечная группа\$
\$\начало группы\$
Находясь в вооруженных силах, а часто и за границей от 2 недель до 6 месяцев, что приводило к выходу из строя автомобильных аккумуляторов, я купил трансформатор переменного напряжения (5 ампер).





 1)
1)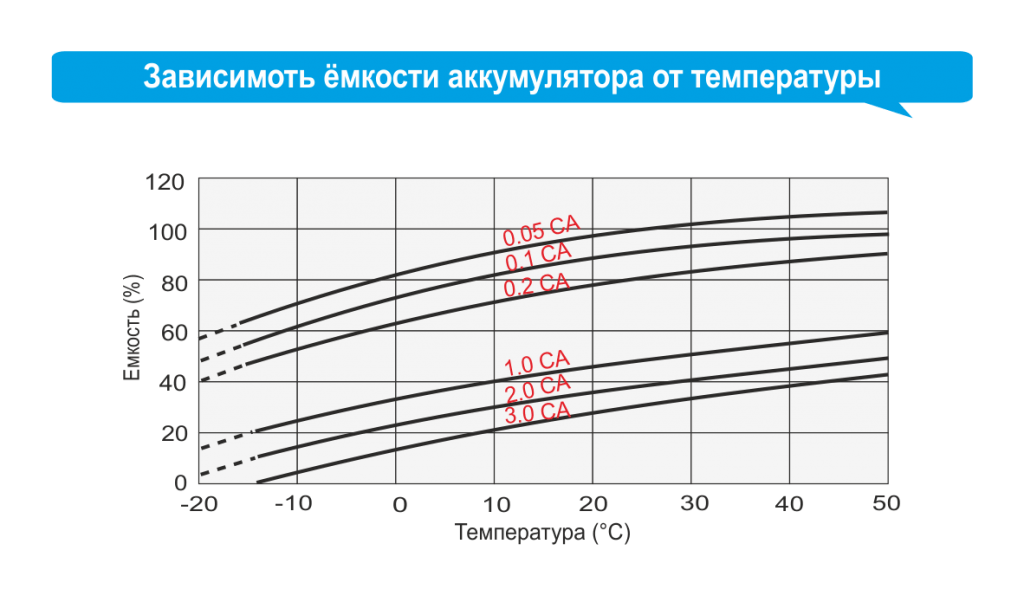 Более теплая среда требует немного более низких порогов напряжения, а холодная окружающая среда предпочитает более высокий уровень.
Более теплая среда требует немного более низких порогов напряжения, а холодная окружающая среда предпочитает более высокий уровень.